填充体积的影响
小规模培养中的操作条件应该被表征并且通常可以转移到更大规模。对于微生物表达系统,最相关的工程参数之一是氧气传递速率。通过简单地改变培养体积,可以改变氧气传递速率。图10给出了填充体积以及因此小规模培养中氧气传递速率影响的一个很好的例子。
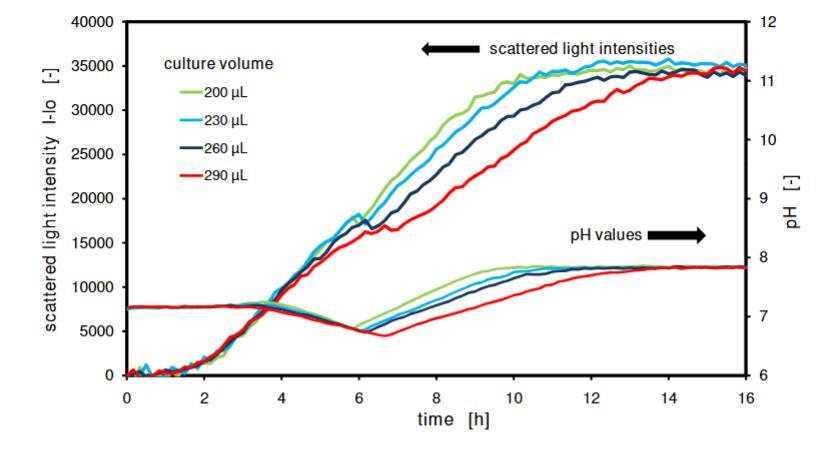
图10:填充体积的影响。填充体积从200 μL到290 μL的大肠杆菌培养物的生长和pH监测;大肠杆菌BL21在TB培养基中培养,在96孔MTP中测量,填充体积为200、230、260和290 μL,温度30°C,摇动频率995 rpm,摇动直径3 mm,散射光(激发:620 nm/发射:-,增益:20),HPTS(激发:410 nm和460 nm/发射:510 nm,增益:10),玻尔兹曼方程校准参数:IR,min=0.00, IR,max=3.00, dpH=0.50, pH0=7.20。
在图10中,在已知为强需氧培养基(OTR~0.07 mol/L/h)的复杂TB培养基中监测了大肠杆菌培养物的生长和pH。在标准96孔MTP中应用了200 μL、230 μL、260 μL和290 μL的不同培养体积。随着培养体积的增加,由于氧气传递速率降低,生长速率降低,发酵时间延长。此外,在较高体积的培养物中,pH下降更为明显,因为在有限的氧气传递条件下,细菌被迫从甘油产生有机酸。在更高的氧限制下产生更多的酸。培养物从甘油到蛋白胨的二次生长转变,反映在生长曲线中部散射光信号的轻微下降,也与pH从下降到上升的趋势转变非常吻合。乍一看,不同的传质条件似乎对最终生物量产率和最终pH没有影响;但是,当然观察到了不同的生长速率和酸化作用。必须考虑到,即使是比这里应用的更差的传质条件和缓冲能力更低的培养基,也可能导致不良影响,例如生物量生长终止或目标产物蛋白的不稳定性。总之,不确定的培养条件可能导致意想不到的选择压力、错误的工艺设计,并最终在放大过程中引起不必要的问题。
这里应用的可溶性荧光pH染料(HPTS)可能是通常昂贵的pH光极的良好替代品。它易于应用于任何类型的微滴度板,并且可以用标准的荧光板读数仪读取。这种方法的主要缺点是研究人员必须自己并在任何新的读数仪上进行密集的校准。相比之下,pH光极通常随校准参数一起提供。
结论
所提出的基于微滴度板的发酵系统可用于定量高达50 g/L细胞干重的微生物生物量浓度,且与离线生物量值呈线性相关,无需任何稀释。这允许在发酵过程中可靠地在线监测生物量发展,而无需取样和稀释。并行监测发酵液中荧光蛋白浓度(例如GFP或其衍生物)或其他荧光分析物,首次允许在线计算生物过程的典型评估标准,例如产率、比生长和产物形成速率以及体积生产率。当然,并非每次产物筛选中都能获得在线产物数据,然而,分子生物学和生物标志物研究的持续发展最终将为荧光报告蛋白创造更广泛的应用。
目前应用的一种解决方案是将GFP或任何其他荧光蛋白与靶蛋白融合。这提供了融合蛋白的荧光信号和在线检测的可能性。融合蛋白表达后,荧光蛋白伴侣可以在下游加工过程中通过特定的蛋白酶从靶蛋白上切割下来。另一个更广泛的方法来评估产物产率是将离线分析数据与在线数据相结合。为此,从微滴度板中进行手动或自动取样将是有帮助的。
为了减少取样频率,从而减少取样过程中移除的体积,可以使用在线生物量信号来触发取样。良好的取样点可能是指数生长期中期、进入稳定期和稳定期末期。结合这些在线监测和离线蛋白质及营养物分析方法,可以为生物过程提供更复杂的信息和评估标准。另一个有趣的代谢物,NADH,也可以用BioLector技术监测。
在有氧和无限制的生长条件下,NADH荧光可以与生物量浓度相关联,而在氧气、pH或营养限制下,该信号可以成为限制或代谢变化的有价值指标。此外,该技术可用于通过比较生物量浓度、比生长速率、产率和产物形成速率等参数来评估不同的培养基。甚至在使用不同碳源的培养基上可以检测到二次生长转变。因此,这种定量方法可以积极地将培养基开发从仅仅是经验性的实验转变为定量和基于知识的培养基设计。
将BioLector技术与现代基因工程相结合,可以直接在培养过程中实时表征启动子等遗传元件与荧光蛋白的结合。通过报告蛋白的荧光,可以轻松研究各种不同的底物、化学化合物和发酵参数。在小规模发酵中一个经常被低估的方面是工程参数的影响。在进行小规模高通量实验时,如果实验结果可以直接转移到更大的反应器规模,那将是最有吸引力的。因此,应针对相关工程参数对微滴度板等小规模反应器进行很好的表征。
常见的48孔和96孔类型微滴度板的OTRmax和kLa值已经被表征。关于用实验室发酵罐数据验证微尺度发酵数据,还需要进一步的工作。本文作者将在不久的将来在另一篇论文中讨论这个放大问题。总之,BioLector技术是一个强大的工具,可以在高通量和定量方式下更深入地了解生物过程。它非常适用于克隆筛选、培养基优化、系统生物学和早期生物工艺开发。该领域的未来研究应将这项技术推向集成用于监测pH、DOT和其他发酵参数的光极。证明其可放大到搅拌釜发酵罐以及扩展到其他细胞类型(如植物、哺乳动物和人类细胞系)是非常可取的。
相关新闻推荐
1、伤寒沙门菌t4606基因缺陷株在高渗应激环境下的生长曲线(二)
2、共同菌根网络(CMNs)改变根际微生物群组装促进植物抗病性的全新机制
