研究简介
细菌抗肿瘤疗法自19世纪Coley博士使用热灭活细菌治疗癌症以来,已取得长足进展。VNP作为减毒沙门氏菌株,在临床前模型中表现出抗肿瘤潜力,但Ⅰ期临床试验因毒性强和疗效低而终止。巨噬细胞作为天然免疫细胞,具有肿瘤趋化特性,并能吞噬病原体后缓慢释放,避免过度免疫反应。本研究假设巨噬细胞介导的VNP递送可降低毒性、提高肿瘤靶向性,并通过工程化VNP表达PD1nb,增强免疫激活效果。本研究旨在解决细菌抗肿瘤疗法中副作用大和疗效有限的问题。细菌疗法如减毒沙门氏菌VNP20009(VNP)因能特异性定植肿瘤并激活免疫而备受关注,但临床应用中易引起肝脾毒性等副作用。论文创新性地提出利用巨噬细胞作为生物载体,实现VNP的肿瘤靶向递送,并结合抗PD1纳米抗体(PD1nb),开发出一种三重免疫疗法(细胞疗法、细菌疗法和免疫检查点阻断疗法),在黑色素瘤模型中显示出显著疗效。
研究人员使用小鼠巨噬细胞系RAW264.7和原代腹膜巨噬细胞(PEM),与VNP菌株(如VNP-RFP或VNP-PD1nb)以1:10比例共培养60分钟,通过庆大霉素处理清除胞外细菌,获得VNP加载的巨噬细胞[MΦ(VNP)]。体外实验评估了巨噬细胞的吞噬效率、VNP存活率、释放行为及对肿瘤细胞(B16F10黑色素瘤细胞)的杀伤作用。体内实验在B16F10荷瘤小鼠模型中,通过尾静脉注射MΦ(VNP)细胞(剂量为1×10^5细胞/鼠),比较其与单独VNP给药的毒性、肿瘤靶向性和疗效。
工程菌VNP-PD1nb通过质粒构建,表达并分泌抗PD1纳米抗体,以阻断PD1/PDL1免疫抑制通路。本研究首次将巨噬细胞作为“特洛伊木马”递送工程细菌,解决了细菌疗法的毒性和靶向性难题,并结合免疫检查点阻断,形成了一种模块化、低剂量(仅需10^5细胞)的高效疗法(Figure 8)。该策略为多重免疫疗法提供了新思路,具有临床转化潜力,尤其在治疗转移性肿瘤方面前景广阔。未来可探索通过基因编辑优化细菌表达调控,进一步减少脱靶效应。
Bioscreen 全自动生长曲线分析仪的应用
将构建好的大肠杆菌互补菌株(携带衣原体 lplA1Ct、lplA2Ct或 lipACt基因的质粒)接种到含有或不含外源硫辛酸(10 µM)的 M9 甘露醇基本培养基中。每个条件下设置 5 个重复,Bioscreen全自动生长曲线分析仪能够自动、连续地监测培养物的光密度(OD),从而生成生长曲线,并计算标准偏差以评估数据的可重复性。通过比较菌株在缺乏外源硫辛酸的培养基中的生长情况,可以判断表达的衣原体基因是否能弥补宿主自身硫辛酸合成或利用途径的缺陷。Bioscreen全自动生长曲线分析仪通过自动化、多重复的监测,将“能否生长”这一生物学问题转化为精确、可比对的生长动力学数据,是连接基因构建(基因型)与功能验证(表型)之间的关键实验桥梁。
实验结果
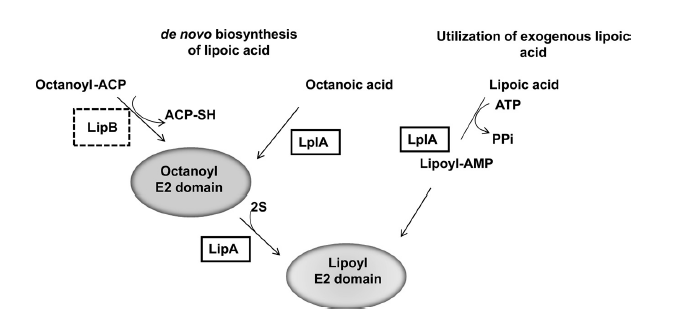
沙眼衣原体L2血清型主要依赖其硫辛酸连接酶LplA1来获取并利用宿主来源的外源硫辛酸,以满足其胞内生长需求,而基因组中编码的硫辛酸合酶(LipA)可能不具备功能。通过蛋白质免疫印迹分析,在沙眼衣原体的原体(EB)和网状体(RB)中均检测到被硫辛酸修饰的蛋白质,其大小与预测的几种关键脱氢酶复合体的E2亚基相符。
利用大肠杆菌作为替代宿主的功能互补实验表明,衣原体的硫辛酸连接酶LplA1Ct具有生物学活性。它能够有效利用外源添加的硫辛酸,恢复因缺失自身连接酶而无法利用外源硫辛酸的大肠杆菌突变株的生长。进一步的体外酶活实验证实,纯化的LplA1Ct蛋白可以直接催化硫辛酸连接到靶蛋白(包括衣原体自身的BCKDH-E2亚基)上。此外,在无外源硫辛酸时,表达LplA1Ct的菌株也能产生脂酰化蛋白,提示该酶可能也能利用内源的辛酸前体。
沙眼衣原体是一种硫辛酸营养缺陷型生物,其存活和生长依赖于从宿主细胞中获取硫辛酸,而这一获取过程主要由LplA1连接酶介导。因此,LplA1酶被认为是开发新型抗衣原体药物的一个潜在靶点。
相关新闻推荐
2、鼠李糖乳杆菌Probio-M9连续传代培养过程中稳定性评价(二)
3、芽孢杆菌对黄曲霉毒素B1、呕吐毒素、玉米赤霉烯酮的降解作用——材料与方法
