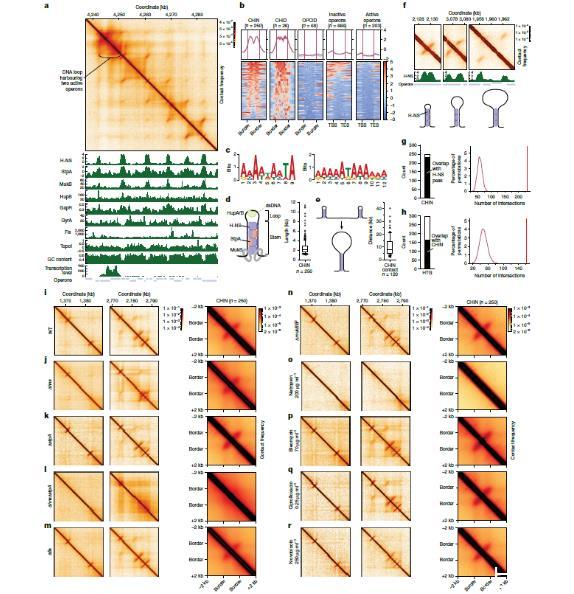
图3、由 H-NS 及其他 NAPs 控制的 CHINs 和 CHIDs 的组织结构。a. 示例接触图,包括 NAP 分布的轮廓、GC 含量、转录信号和操纵子轨迹。b. H-NS 在 CHINs、CHIDs、OPCID、非活性操纵子和活性操纵子周围的位置分布。注释与图 2b 一致。c. 来自 PRODORIC 数据库的 H-NS 基序(左)与通过 HOMER 识别的 CHIN 基序(右)。d. 描述单个 CHIN 组织结构的模型,展示了 CHIN 长度分布(右;n 表示评估的 CHIN 数量)。dsDNA,双链 DNA。
e. 两个 CHIN 之间相互作用的模型,它们展开并融合形成一个大环的茎部。CHIN 之间相互作用的距离分布也展示出来(右;n 表示评估的 CHIN 接触数量)。箱形图从第 25 百分位数延伸至第 75 百分位数,边框向下延伸至第 10 百分位数,向上延伸至第 90 百分位数,中心线表示中位数(d,e)。f. H-NS 在 CHIN 茎区域内的定位,显示在 CHIN 茎处有峰值。g. 与 H-NS 峰重叠的 CHIN 数量。h. 与 CHIN 重叠的 HTG 数量。i - r,分别为野生型大肠杆菌细胞中两个典型携带 CHIN 区域的接触图(i)以及在缺失了指定基因的菌株(j - n)或在使用抗生素处理的野生型细胞(o - r)中相同区域的接触图,展示了 Δhns 细胞中 CHIN 的重新排列以及 ΔhnsΔstpA 和网罗霉素处理细胞中完全的 CHIN 解体。
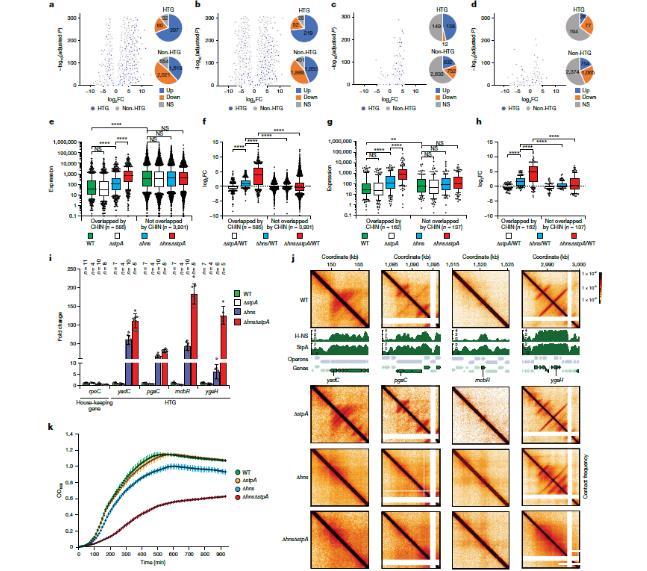
图4、在 H-NS 和双 hns stpA 基因敲除的条件下,热激基因(HTGs)的激活情况。a - d,通过 RNA 测序确定的 hns 和 stpA 缺失后基因表达的变化(a),暴露于 200 µg ml−1 的净罗普辛(b),hns 缺失(c)和 stpA 缺失(d)。此外,还展示了在 Δhns、ΔstpA、ΔhnsΔstpA 和净罗普辛处理的 E. coli 细胞中上调、下调或无显著变化的 HTGs 和非 HTGs 的分布情况。P 值是使用双侧 Wald 检验计算的,并通过 Benjamini-Hochberg 校正进行多重检验调整,假发现率设为 0.05。FC,倍数变化。e,与 WT E. coli 细胞中重叠的 CHIN 基因和不重叠的 CHIN 基因的表达水平(绿色)与 Δhns(蓝色)、ΔstpA(白色)和 ΔhnsΔstpA(红色)中的相同基因组的表达水平进行比较。
f,响应 Δhns、ΔstpA 和 ΔhnsΔstpA 的 CHIN 相关和 CHIN 不相关基因的表达变化。g、h,与 e 和 f 类似,但特别关注 HTGs。所涉及的基因数量(n)已标明。箱形图从第 25 百分位数延伸至第 75 百分位数,边框向下延伸至第 10 百分位数,向上延伸至第 90 百分位数。而中心线则代表中位数。i、选定的热激基因(HTGs)在 Δhns、ΔstpA 和 ΔhnsΔstpA 条件下的表达变化,通过 RT-qPCR 测定。信号以 16S rRNA 为参照进行标准化,其中野生型细胞中的表达水平被设定为 1。1. 数据以平均值±标准差的形式呈现。j, 微孔接触图展示了在野生型、ΔstpA、Δhns 和 ΔhnsΔstpA 细胞中被选作 RT-qPCR 分析的含有 HTG 的区域的图像。 k,使用 Bioscreen 测量的野生型、ΔstpA、Δhns 和 ΔhnsΔstpA 大肠杆菌细胞的生长速率。数据以平均值±标准差的形式呈现,其中野生型、ΔstpA 和 Δhns 的 n = 7 个生物学重复样本,而 ΔhnsΔstpA 的 n = 14 个样本。OD600,600 纳米处的光密度。
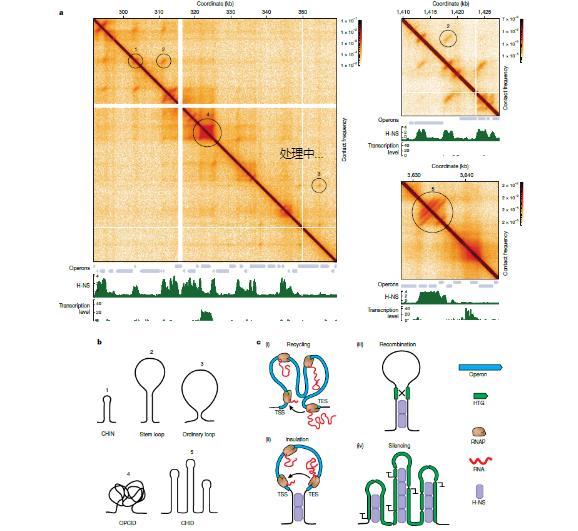
图5、微-芯片技术在大肠杆菌基因组中所捕捉到的初级结构和更高层次结构。a. 来自野生型大肠杆菌细胞的示例接触图谱,展示了各种接触模式。b. 不同接触模式的解释。c. 在本研究中所绘制的 OPCIDs 和 CHIN 网络能够通过将启动子(起始密码子)和终止子(终止密码子)置于接近位置来促进 RNA 聚合酶的回收(i 和 ii)。它们还能建立活跃操纵子的空间隔离(ii),实现远距离高度转录基因之间的重组(iii)并促进高度转录基因的沉默(iv)。
总结
本研究通过开发分辨率高达10碱基对的增强型Micro-C技术,首次在超高分辨率下揭示了大肠杆菌基因组由两类功能对立的基础三维结构单元构成的全新组织框架。研究发现,组蛋白样蛋白H-NS及其旁系同源蛋白StpA 在富含AT的非转录区(尤其是水平转移基因所在位置)组装形成了一类全新的染色体发夹结构及其染色体发夹结构域,这些结构作为物理框架直接介导了外源基因的空间沉默,其解离会导致基因激活与生长延迟。与此同时,所有活跃转录的操纵子会形成严格依赖转录活性的、边界清晰的操纵子尺度染色质互作域,其最显著的特征是启动子与终止子间的高频空间接触,这可能为RNA聚合酶的回收和高效转录提供了空间基础。
该工作将细菌基因组的精细三维架构与具体的转录激活、外源基因沉默等核心生物学功能直接联系起来,为理解细菌的适应性与进化提供了全新的三维空间视角。Bioscreen C全自动生长曲线分析仪被用于精确量化不同基因型大肠杆菌(如Δhns、ΔstpA及ΔhnsΔstpA)的生长表型。具体操作是将预处理后的细菌培养物稀释并加样至仪器的蜂窝板中,于37°C下持续振荡培养,仪器每10分钟自动测量一次OD600值,从而生成高时间分辨率的生长曲线。通过对比生长曲线,研究直观地证实了H-NS/StpA双敲除(ΔhnsΔstpA)会导致显著的生长延迟。这一关键的生理学表型数据,与分子层面观察到的染色体发夹结构(CHINs/CHIDs)完全解体和水平转移基因(HTGs)激活的现象直接对应,为“H-NS/StpA通过维持特定三维基因组结构来沉默外源基因、保障正常细胞生长”这一核心结论提供了不可或缺的实验证据。 。
相关新闻推荐
3、最佳培养条件下沙福芽胞杆菌生长曲线与CA活性曲线测定及研究(二)
