研究简介
本研究开发并应用一种分辨率高达10碱基对的增强型Micro-C染色体构象捕获技术,首次在超高分辨率下揭示了大肠杆菌基因组复杂而有序的三维组织结构,发现了两类全新的基础空间结构单元,并阐明了它们与基因转录调控和基因组稳定性的直接功能联系。长期以来,由于Hi-C等技术的分辨率限制(通常为0.5-1 kb),细菌拟核的精细三维结构及其功能组织机制一直不甚明晰。本研究的核心突破在于通过优化Micro-C实验流程(包括双交联、避免使用去垢剂等),成功绘制了迄今分辨率最高的大肠杆菌基因组空间互作图谱,从而能够观察到此前无法探测的细节。
研究发现了一类全新的空间结构——染色体发夹结构及其组成的染色体发夹结构域。这些结构特异性地形成于基因组中非转录的、富含AT的区域,并且与水平转移基因的基因组位置高度重合。组蛋白样蛋白H-NS及其旁系同源蛋白StpA是组装和维持这些发夹结构的关键因子。CHINs和CHIDs充当了基因沉默的物理框架:当敲除hns和stpA基因,或使用药物Netropsin竞争性结合AT-rich DNA时,这些发夹结构会完全解离,导致其内部沉默的水平转移基因被大量激活,并伴随细菌生长延迟。OPCID的形成严格依赖于转录活性,在热激激活相应操纵子时出现,而被利福平抑制转录时则消失。
与之前报道的转录相关结构不同,OPCID在接触图上呈“方形”模式,且其最显著的特征是启动子与终止子之间存在高频的空间接触,这种接触强度与转录水平正相关,提示了一种通过空间邻近性促进RNA聚合酶回收、以维持高效转录输出的新机制。本研究刷新了对原核基因组三维结构的认知,揭示了大肠杆菌拟核是由“活跃”的OPCIDs和“沉默”的CHINs/CHIDs这两类功能迥异的基本单元共同构成的。该框架将基因组空间架构与具体的生物学功能(转录激活与外源基因沉默)直接关联,并为理解细菌适应性与进化(如水平转移基因的重组)提供了新的三维空间视角。
Bioscreen 全自动微生物生长曲线分析仪的应用
Bioscreen C全自动生长曲线分析仪作为关键的表型监测工具,具有无蒸发、无早熟,可连续测量1600小时,同时测量三个波段的特点,被用于量化不同基因型大肠杆菌突变体(如Δhns、ΔstpA、ΔhnsΔstpA)以及经药物(如利福平、博来霉素)处理后的细菌生长动力学,从而将微观的三维基因组结构变化与宏观的生理表型直接关联。研究人员将预处理后的细菌培养物稀释并加样至仪器的蜂窝板中,在37°C下持续振荡培养,仪器每10分钟自动测量一次OD600值,并绘制高时间分辨率的生长曲线。通过对比野生型与突变体的生长曲线,研究直观地证明了H-NS/StpA双敲除(ΔhnsΔstpA)会导致细菌出现明显的生长延迟。这一生长缺陷的表型,与分子水平上观察到的染色体发夹结构(CHINs)和染色体发夹结构域(CHIDs)完全解体、以及水平转移基因(HTGs)转录激活的现象相互印证,为“H-NS/StpA蛋白通过组装CHINs/CHIDs来维持基因组三维结构稳定性,进而沉默外源基因、保障正常生长”这一核心结论提供了至关重要的生理学证据。
实验结果
研究发现了一类全新的空间结构——染色体发夹结构及其组成的染色体发夹结构域。这些结构特异性地形成于基因组中非转录的、富含AT的区域,并且与水平转移基因的基因组位置高度重合。组蛋白样蛋白H-NS及其旁系同源蛋白StpA是组装和维持这些发夹结构的关键因子。CHINs和CHIDs充当了基因沉默的物理框架:当敲除hns和stpA基因,或使用药物Netropsin竞争性结合AT-rich DNA时,这些发夹结构会完全解离,导致其内部沉默的水平转移基因被大量激活,并伴随细菌生长延迟。
这证明CHINs/CHIDs是H-NS介导的外源基因沉默在三维空间中的具体实现形式。所有活跃转录的操纵子都会形成一个大小与操纵子匹配、边界清晰的操纵子尺度染色质互作域。OPCID的形成严格依赖于转录活性,在热激激活相应操纵子时出现,而被利福平抑制转录时则消失。与之前报道的转录相关结构不同,OPCID在接触图上呈“方形”模式,且其最显著的特征是启动子与终止子之间存在高频的空间接触,这种接触强度与转录水平正相关,提示了一种通过空间邻近性促进RNA聚合酶回收、以维持高效转录输出的新机制。
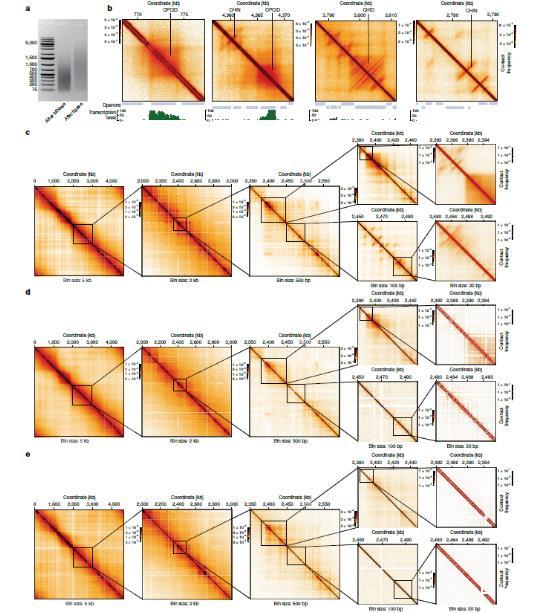
图1、超高分辨率的微芯片图谱揭示了大肠杆菌基因组复杂的三维结构。a,经过微芯片操作的不同步骤后 DNA 的琼脂糖凝胶电泳图,展示了进行超高分辨率图谱绘制所需的片段化模式(未裁剪的凝胶图见补充图 1)。由于大肠杆菌缺乏核小体,MNase 不会产生典型的 200 个碱基对的 DNA 梯状结构,而是产生一系列片段的混合物。所有的微芯片实验都经过测试以显示相似的分离模式。b,微芯片接触图示例,展示了 OPCIDs、CHINs 和 CHIDs 以及转录活性图谱和操纵子轨迹。c–e,微芯片与 Hi-C 数据的比较:来自正常生长条件下野生型大肠杆菌细胞的微芯片图谱(c);使用相同细胞按照标准 Hi-C 方法生成的 Hi-C 接触图谱(d);以及之前发表的 8,55 份大肠杆菌 MG1655 的 Hi-C 图谱(e)。左侧图幅展示全基因组视图。注意 在 Hi-C 技术中将测序片段的大小减小到 500 个碱基以下并不会显著提高分辨率,而 Micro-C 技术所生成的图谱则能展现出更为精细的细节,尤其是在亚千碱基的分辨率水平上。
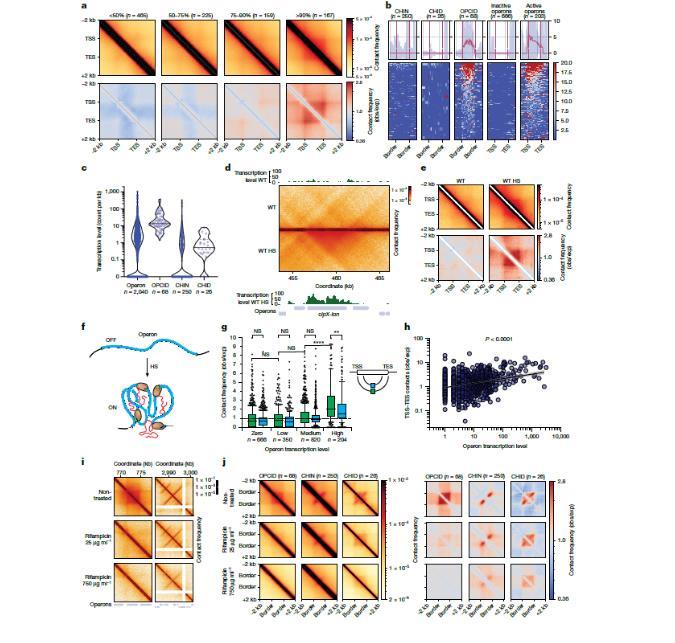
图2、在活跃的操纵子上存在由转录驱动的 OPCIDs(操纵子旁结构域),而在被抑制的基因区域中存在与转录无关的 CHINs(转录抑制结构域)和 CHIDs(转录抑制结构域的内部区域)。a. 基于红-C 信号对按转录活性分组的操纵子的平均接触图。b. CHINs、CHIDs、OPCID、非活跃操纵子(红-C 信号为零)和活跃操纵子(红-C 信号前 10%)周围的转录水平。上方堆积的曲线代表中位信号,阴影区域表示自助标准误差。c. 按特定基因特征内转录水平的标准化,以特征长度为基准。实线和虚线分别代表中位数和 25%至 75%的百分位数。d. 包含热休克(HS)操纵子 clpX-lon 的正常和 HS 条件下的接触图。e. 在正常和 HS 条件下 σ32 操纵子的平均接触图。n = 26。f. 说明在 HS 条件下通过转录激活将操纵子组装成 OPCID 的示意图。
g. 按照红-C 信号将操纵子分组为未转录(红-C 信号为零)、低转录(排除零后底部 50%)中等转录(50%-90%)和高转录(顶部 10%)的转录子的启动子-终止子接触频率。n 表示。每组中的操纵子数量。此外还展示了内部操纵子区域之间的接触频率:一个位于启动子起始序列下游 20% 处,另一个位于终止子上游 20% 处。箱形图从第 25 百分位数延伸至第 75 百分位数,边框向下延伸至第 10 百分位数,向上延伸至第 90 百分位数,中心线表示中位数。P 值是通过单因素方差分析计算得出的,然后进行图基多重比较检验。h,操纵子转录水平与启动子-终止子接触频率之间的相关性。i,两个代表性区域的接触图,分别在使用 25 µg ml−1 或 750 µg ml−1 的利福霉素处理之前和之后展示。j,低(25 µg ml−1)或高(750 µg ml−1)浓度利福霉素处理前后 OPCID、CHIN 和 CHID 的平均接触图,说明转录抑制对这些基因结构的影响。
相关新闻推荐
1、不同温度、盐度、pH、碳源、氮源对嗜水气单胞菌的生长影响(二)
