大肠杆菌在土壤中的存活与土壤微生物群落的复杂度呈负相关。在未添加BS3的新鲜土壤中,大肠杆菌计数逐渐下降,在75-120天孵育后降至检测水平以下(如图3所示)。新鲜土壤中大杆菌的衰减速率范围为0.056至0.102天⁻¹,平均k值为0.072天⁻¹(表3)。这些衰减速率在其他研究者报告的数值范围内,他们表明衰减速率通常在各类土壤的0.02-0.238范围内。虽然在0.05% BS3处理中大肠杆菌比新鲜土壤中死亡更快,但在0.15%、0.30%和0.50% BS3处理中大肠杆菌的衰减显著减慢。除0.50% BS3外,平均死亡速率随BS3密度的增加而逐渐下降。在0.30% BS3处理中观察到的最低平均k值仅为新鲜土壤中的68%。在0.50% BS3处理中,平均死亡速率比0.30% BS3中高10%。
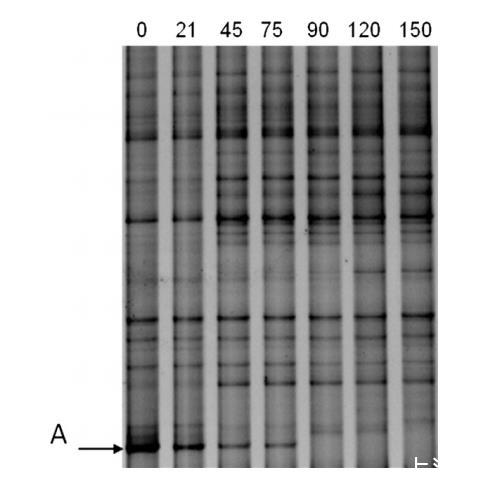
图4.经0.3%BS3处理并接种土壤来源大肠杆菌的土壤 DGGE 指纹图谱。凝胶图谱顶部数字表示培养时间(天)。
土壤中大肠杆菌的存活模式通过土壤细菌群落的DGGE条带图谱清晰可视化。例如,在接种土壤来源大肠杆菌的0.30% BS3处理土壤的DGGE图谱上(如图4所示),一个清晰的条带(标记为条带A)存在于接种土壤中,而在未接种土壤中不存在,该条带在0天时采集。对该条带进行测序并确认与该土壤大肠杆菌菌株的16S rRNA序列片段100%相同。因此,该条带在DGGE图谱上的存在表明该大肠杆菌菌株的存在。该条带的强度随孵育时间降低,在90天及以后变得不可见。其他处理的DGGE图谱具有相似的趋势,但大肠杆菌指示条带不可检测的时间不同。该条带在新鲜土壤和接种狗大肠杆菌的0.05% BS3土壤中孵育45天后不可检测。对于其他土壤处理+大肠杆菌组合,通常在75或90天孵育后该条带变得不可见。该条带在120天孵育后无法在所有样品中检测到(数据未显示)。
| 土壤处理a | 人 | 土壤 | 狗 | 平均值 |
|---|---|---|---|---|
| 新鲜 | 0.056 | 0.059 | 0.101 | 0.072 |
| 0.05% BS3 | 0.064 | 0.049 | 0.120 | 0.078 |
| 0.15% BS3 | 0.045 | 0.051 | 0.091 | 0.062 |
| 0.3% BS3 | 0.041 | 0.047 | 0.061 | 0.050 |
| 0.5% BS3 | 0.043 | 0.050 | 0.071 | 0.055 |
| 灭菌 | 0.051 | 0.046 | 0.086 | 0.061 |
4. 讨论
本研究旨在评估大肠杆菌菌株在微生物群落逐渐改变的砂质土壤中的存活特征,在微宇宙设置中,当其他生物和非生物因素在处理之间保持相似时。实际上,这消除了其他因素对接种大肠杆菌进入新栖息地持久性的影响。大肠杆菌菌株分离自三个来源并在实验室培养,以提供相对可比的接种密度。本研究获得的结果表明,所有三种大肠杆菌菌株在细菌群落减少的土壤中倾向于存活更好。
4.1 BS3对微生物群落组成的影响
Byappanahalli和Fujioka发现,向土壤微宇宙添加BS3导致11天孵育后土壤可培养细菌损失94%至99%。在我们的研究中,证明BS3添加不仅显著降低了细菌数量,还强烈改变了土壤微生物群落的组成,这一点通过培养依赖和培养非依赖方法都清楚显示。第10天BS3处理土壤中CD值的增加可能表明BS3诱导部分细菌进入生理非活跃状态,如孢子或VBNC,这反过来缓解了对营养物质的竞争,从而增加了适应BS3存在的细菌的丰度。适应BS3的可能机制包括诱导外排泵基因的过度表达,这对细胞内代谢物解毒过程很重要。估计约5-10%的所有细菌基因参与转运,其中很大一部分编码外排泵。非特异性外排泵可能将一系列结构不同的化合物从细胞内转运到外部环境。这些外排泵基因可能通过适应性突变或水平基因转移获得。
与培养法获得的数据不同,通过扩增16S rRNA片段的DGGE分析,在第10天仅检测到BS3添加引起的细菌群落组成的轻微变化。VBNC细菌中的DNA可能仍可使用DGGE提取和指纹分析。细胞衰变后附着在土壤颗粒上的可提取DNA的持久性也可能有助于第10天不同处理之间DGGE图谱的相似性。仅在第90天,DGGE揭示了更明显的按处理聚类。培养法和分子法数据之间的差异可能归因于这两种方法识别两种不同谱系的微生物这一事实。培养法仅检测在特定孵育条件下在培养基上生长并形成菌落的微生物。大多数土壤细菌无法在培养中生长:估计只有1%的总细菌可以在实验室培养基中常规培养。分子技术依赖于从复杂土壤基质中的可培养和不可培养微生物有效提取核酸,应该能够检测更广泛的土壤微生物谱系。然而,由于抑制物质的存在、不同的扩增效率和/或胞外DNA的共扩增,基于DNA的方法经常引入偏差。
本研究中使用的BS3浓度(0.05-0.5%)与培养基中使用的浓度(0.15%)相当,低于人肠道中BS3的上限水平。虽然BS3可能在体内和体外被一些严格厌氧肠道细菌降解,但我们研究中的孵育条件不适合BS3的快速降解。此外,BS3的分解受底物抑制,当BS3水平达到0.50%时,即使其他条件保持优化,也检测到很少的反应。因此,在本研究中,BS3对细菌生长的抑制和细菌群落的改变可能在土壤微宇宙中持续很长时间。这与熏蒸对土壤生物学性质的影响不同,后者通常一次性起作用,导致来自裂解细胞的暂时增强的营养物质可利用性和氯仿的快速生长。
相关新闻推荐
2、共同菌根网络(CMNs)改变根际微生物群组装促进植物抗病性的全新机制
