摘要
目的: 本研究的目的是确定并追踪医院废水管道沉淀物中粪便细菌对抗菌药物的耐药性随时间的变化。进一步的目标是测定敏感型、中间型和耐药型肠道肠球菌在不同环丙沙星浓度中的生长速率,作为细菌适应性的衡量指标。
方法: 在卡尔马县医院安装了一个能够随时间收集沉降颗粒的系统。在14个月期间每两个月采集一次样本。采用标准方法从沉淀物中分离大肠菌群细菌和肠球菌,并通过纸片扩散法检测其对环丙沙星(CIP)、亚胺培南(IMI)、甲氧苄啶-磺胺甲噁唑(TS)、氨苄西林(AMP)和万古霉素(VAN)的耐药性。耐药分离株进一步使用PhenePlate™系统进行分型。生长评估使用全自动微生物生长曲线分析仪Bioscreen C进行。
结果: 肠道肠球菌的耐药率分别为:万古霉素<0.6%、亚胺培南1.3%、氨苄西林1.9%、环丙沙星13%。大肠菌群细菌的耐药率分别为:环丙沙星1.1%、亚胺培南2.2%、甲氧苄啶-磺胺甲噁唑2.2%。在两个采样时间点,发现显著更高比例的环丙沙星耐药肠球菌,PhP分析表明耐药克隆在下水道中已建立。环丙沙星耐药肠道肠球菌的滞后期显著长于敏感分离株,但从500 mg ml⁻¹(半MIC)开始,耐药分离株在世代时间方面具有显著的竞争优势。
讨论: 尽管沉淀物中抗菌药物浓度很高,耐药率普遍较低。这可能取决于粪便细菌有限的生长可能性。然而,耐药克隆的建立表明医院下水道可作为耐药细菌的储存库。
引言
口服抗菌药物摄入后主要排泄到废水中。有些完全以未改变形式排泄,而另一些则通过螯合结合、降解或宿主体内外代谢系统的灭活而或多或少被修饰。抗菌药物排泄与高微生物生物量和丰富的营养物相结合,使废水成为水平基因转移和抗菌耐药细菌选择的潜在栖息地。尽管由于废水稀释,抗菌药物浓度通常太低而无法抑制生长,敏感细菌可能受到影响,导致耐药细菌的选择。一些研究检测到废水处理过程中耐药性增加,而另一些则检测到减少。然而,污水管道也含有沉降颗粒。这种沉降颗粒沉淀物形成一个动态生态系统,其中疏水性化学物质被富集。
在Petersen等人的研究中,在接受家禽和猪粪作为肥料的综合鱼塘中,不动杆菌和肠球菌在沉积物-水界面的耐药性增加。这些粪便来自常规饲喂抗菌药物作为生长促进剂的牲畜。耐药性的增加被解释为耐药细菌的引入或池塘环境中抗菌药物的选择压力。
在另一项鱼塘研究中,土霉素耐药性最初在沉积物细菌中增加,然后在抗菌治疗结束后33至73天之间再次下降。如果沉积物持续暴露于抗生素,例如在医院废水系统中,耐药性发展的风险可能会增加,因为下水道沉淀物中抗菌药物的富集可以形成对细菌群体选择压力的微生态位。一项关于抗菌药物降解和遗传毒性的研究表明,测试的化合物(环丙沙星、氧氟沙星和甲硝唑)均未被生物降解。因此,医院下水道可能作为耐药细菌的环境储存库。
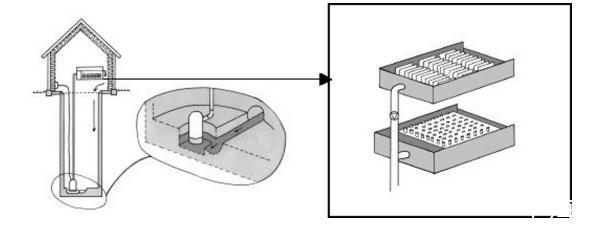
图1. 卡尔马县医院污水管道中的取样装置。取样设备安装于检查井内。废水从检查井底部低于主沟的集水坑中泵出,以确保集水坑内持续存在水体。沉淀颗粒在储罐中通过试管收集。
因此,开发了一个系统来研究医院废水中耐药性发展和抗菌药物浓度的动态(图1)。本报告研究的具体目的是确定粪便指示菌对医院常用抗菌药物的耐药性,并在60周内追踪耐药性发展。进一步的研究确定了被分类为耐药、敏感和中间的细菌分离株的世代时间和滞后期。
材料与方法
在卡尔马县医院新建病区(127张床位:72张普通外科和泌尿外科、33张妇科、22张儿科)的主污水管道中,安装了一个能够在选定间隔对废水中的生物膜和截留沉淀物进行化学和微生物采样的装置,该装置位于4米深的检查井中。废水从横向放置于主管道底部以下的集水坑泵入测试罐,固体内容物在采样管中沉降(图1)。持续监测供水数据,医院药房记录每个病房使用的抗生素数量。这些研究的结果已由Jarnheimer等人发表。
细菌采样与分离
在14个月期间每两个月进行一次采样。收集三个试管并运输到实验室。按照Långmark等人的描述,将10克沉降沉淀物与90毫升含0.5%吐温80的磷酸盐缓冲盐水(PBS)在Stomacher中混合。提取物进行连续稀释,通过标准方法分离肠道肠球菌和大肠菌群细菌的菌落。简要地说,从适当稀释度取0.1毫升涂布于m-Endo琼脂LES,在35°C下孵育21±3小时。典型金属光泽菌落进一步检测氧化酶产生,氧化酶阴性菌落确认为大肠菌群细菌。为分离肠道肠球菌,将0.1毫升涂布于m-Enterococcus琼脂,在35°C下孵育44±4小时。典型深红色菌落通过其在44°C下发酵七叶苷的能力验证为肠道肠球菌。
相关新闻推荐
1、全自动微生物生长曲线分析仪应用:黄芩素与壳聚糖抑制酵母生物膜研究(一)
3、微生物生长曲线分析仪评估化合物C6抑制剂对单核细胞增生李斯特菌的直接抗菌活性
