EPS分离和定量
遵循方案区分与细胞结合的胞外多糖和释放到培养基中的胞外多糖。通过乙醇沉淀从培养上清液中沉淀,而结合型EPS则先用EDTA从细菌细胞中提取,再进行乙醇沉淀。为比较不同培养基中的EPS产量,EPS量表示为每菌落形成单位产生的葡萄糖当量。
DNA操作
常规分子生物学技术按照标准程序进行。限制性内切酶和修饰酶按制造商推荐使用。质粒DNA通过QIAGEN小量制备试剂盒制备。染色体DNA和质粒DNA的分离如前所述。
鼠李糖乳杆菌GG wzb基因的克隆
设计引物基于已发表的wzb序列鉴定鼠李糖乳杆菌GG的wzb基因。将PCR产物克隆到pCRII-TOPO载体中并测序。通过BLASTx分析,鉴定出一个可能编码鼠李糖乳杆菌GG磷酸酪氨酸磷酸酶Wzb的DNA片段。
wzb反义RNA表达质粒pCMPG5344的构建
为了实现反义RNA的过表达,将wzb基因反向克隆到由组成型启动子控制的高拷贝载体中。将含有启动子和反向wzb基因的片段克隆到高拷贝载体pLAB1301中,得到质粒pCMPG5344。将该载体转入鼠李糖乳杆菌GG。通过Northern印迹分析确认反义RNA的存在。
核苷酸序列登录号
推定的wzb基因序列已提交至NCBI数据库。
结果
鼠李糖乳杆菌GG的体外生物膜形成
使用微孔板形式测定生物膜形成。测试了三种不同的生长培养基:标准MRS培养基、改良TSB培养基和乳杆菌AOAC培养基。在MRS培养基中24至96小时内未观察到生物膜形成。在mTSB培养基中生长72小时后可观察到融合的生物膜生长。此外,鼠李糖乳杆菌GG能够在AOAC培养基中形成生物膜,但不如在mTSB培养基中显著。生物膜在微好氧和厌氧条件下均可形成。鼠李糖乳杆菌GG的生物膜形成也可在带负电荷的玻璃表面上观察到。
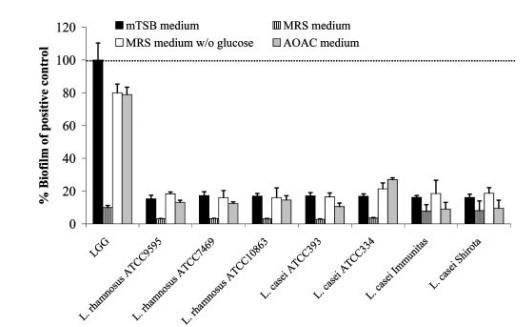
图1.不同乳酸杆菌菌株生物膜形成能力对比。研究比较了八种乳酸杆菌菌株在不同培养条件下的生物膜形成能力,实验条件包括:mTSB培养基、含/不含葡萄糖的MRS培养基以及 AOAC 培养基。结果以鼠李糖乳杆菌GG菌株在mTSB培养基中的生物膜形成能力(阳性对照)为基准值(虚线标示100%),误差线代表八次生物学重复的标准偏差。所示数据至少来自三次独立实验。
不同乳杆菌菌株生物膜形成的差异比较
为了检测乳杆菌菌株在生物膜形成上可能存在的差异,我们选择了干酪乳杆菌群的七个密切相关菌株进行比较研究。选择在生物膜测定所用不同培养基中浮游生长速率相当的菌株。鼠李糖乳杆菌和相关干酪乳杆菌菌株的体外生物膜形成能力差异很大。在所有测试条件下,鼠李糖乳杆菌GG在聚苯乙烯上显示出最好的生物膜形成特性。
生长培养基成分的影响
由于鼠李糖乳杆菌GG在标准MRS培养基中不形成生物膜,因此研究了一些关键成分的影响。系统地省略MRS培养基中的成分,并用其补充mTSB培养基。当从MRS培养基中省略葡萄糖时,可以观察到生物膜形成。葡萄糖的这种生物膜抑制效应通过向mTSB培养基中添加葡萄糖得到证实,这导致生物膜形成减少。与鼠李糖乳杆菌GG相反,其他鼠李糖乳杆菌和干酪乳杆菌菌株在无葡萄糖的MRS培养基中未观察到生物膜形成。
已知二价阳离子通过直接影响静电相互作用来影响细菌粘附。MnSO4对生物膜形成有抑制作用,而MgSO4对生物膜形成没有主要影响。这种差异很可能是由于不同的生长刺激效应。MRS培养基中存在的表面活性剂Tween 80也抑制了生物膜形成。然而,Tween 80的效果似乎是培养基特异性的,因为将其添加到mTSB培养基中并未减少鼠李糖乳杆菌GG的生物膜形成。
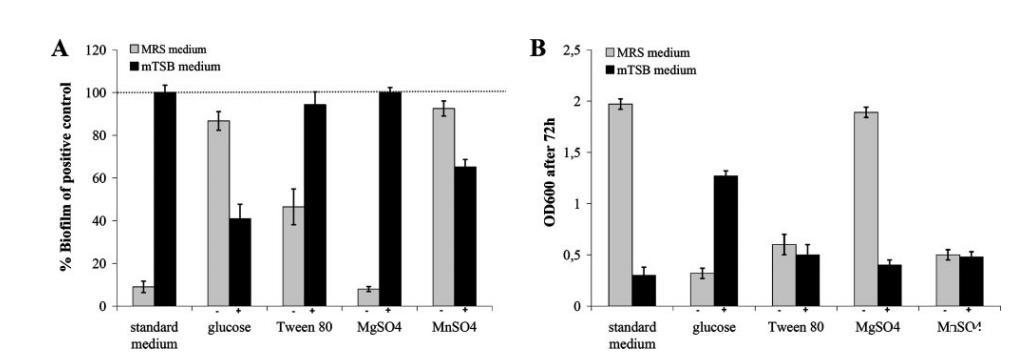
图2. MRS培养基成分对鼠李糖乳杆菌GG生物膜形成的影响 (A) 通过去除MRS培养基中的不同组分(-),探究其对生物膜形成的影响。同时,将这些组分以与MRS培养基相同浓度添加至mTSB培养基中(+),进一步研究其作用效果。实验结果以鼠李糖乳杆菌GG在mTSB培养基中形成的生物膜量(阳性对照)为基准(虚线表示100%),进行相对比较。(B) 通过去除MRS培养基中的相同组分(-)及添加至mTSB培养基(+)后,观察这些组分对悬浮培养72小时菌体生长量(OD600)的影响。
相关新闻推荐
2、微生物的分离培养方法、操作步骤及注意事项——划线分离法、涂布平板法
