大肠杆菌在不同培养基中的比较
为了证明BioLector在培养基筛选中的适用性,也使用大肠杆菌进行了培养基比较。研究了在大肠杆菌标准培养基:LB、TB和WR(后者是一种合成补料分批发酵培养基)上的生长和FbFP(荧光蛋白)的表达。图6展示了本实验的结果。
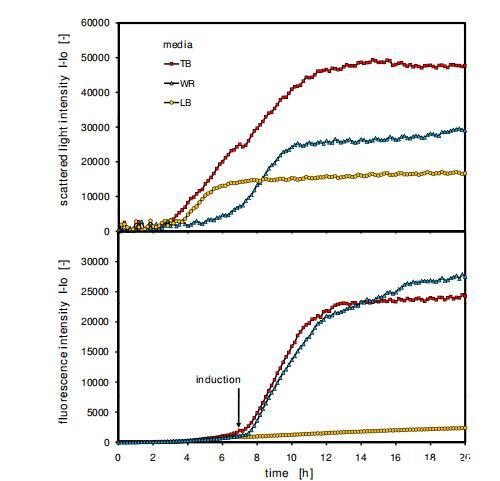
图6:不同培养基的比较-大肠杆菌中基于黄素单核苷酸(FMN)的荧光蛋白(FbFP)的生长和蛋白质表达。大肠杆菌BL21-Pet 28A ytvAC62A在LB、TB和WR培养基中的培养物;在96孔MTP中测量,填充体积200μL,温度30°C,摇动频率995 rpm,摇动直径3 mm,在7.3小时用0.5 mM IPTG诱导,散射光(激发:620 nm/发射:-,增益:20),FbFP(激发:460 nm/发射:520 nm,增益:10)。
有趣的是,在这个实验中可以看到生物量发展的明显差异。大肠杆菌在TB培养基上生长到最高的生物量浓度,而在WR培养基上达到最大浓度的一半,在LB上达到最大浓度的1/3。虽然在WR培养基上观察到典型的指数生长曲线,但在LB和TB培养基上的培养物仅显示线性斜率。此外,在7小时时显示了TB培养基上生长的转变。这先前已被Losen等人描述过,并可能与从甘油到蛋白胨的碳源转变有关。此转变也体现在pH从下降到上升的转折点上。由于复杂培养基中关键中间体和生长构建块的可用性,细胞在复杂培养基(LB和TB)上的生长速度比在合成培养基上快得多。关于该培养基中的蛋白质表达,值得注意的是,尽管在LB培养基中FbFP的表达非常低,但TB培养基中FbFP的表达显著高于LB培养基中的生物量水平。这也可以归因于LB培养物的诱导时间较晚。在诱导时(7.3小时),培养物已经进入稳定生长期,并且没有剩余的碳源来产生蛋白质。在所有培养基诱导前,仅观察到较小的荧光强度,这可以解释为细胞的生物源荧光或FbFP的微小组成型表达。诱导后,启动子被激活,TB和WR培养基中FbFP的荧光强烈增加。
通过使用不同的碳源数量、培养基背景和缓冲条件,可以看到生物量浓度和生长速率的明显差异。通过这些结果,证实了BioLector技术在定量生物量和荧光蛋白监测以及培养基筛选方面的适用性。
克隆筛选
然后将BioLector应用于使用表达GFP作为简化量化模型蛋白的多形汉逊酵母进行克隆筛选。将克隆传代8次以使GFP基因整合到汉逊酵母基因组中,然后稳定。筛选以甘油作为唯一碳源进行;这意味着所应用的FMD和MOX启动子被去阻遏,因此它们主动表达GFP。
图7展示了90个不同克隆的筛选结果。在96孔微滴度板中的分批发酵过程中监测了散射光和GFP的荧光。大多数克隆呈指数生长,大多数克隆在8到13小时之间进入稳定期。大约七个克隆显示出显著降低的生长速率,并在15小时及更晚进入稳定期。两个菌株不生长,与两个未接种培养基的孔一起形成基线。值得注意的是,不同的克隆达到不同的生物量产率,这体现在不同的散射光强度上。由于测量装置的标准差小于5%,稳定期散射光信号中位数周围+/- 15%的偏差表明生物量产率存在显著差异。图7B说明了GFP形成动力学的巨大多样性以及GFP表达水平从几千荧光单位(FU)到30,000 FU的范围。可以假设,在表达真实靶蛋白而非GFP的情况下,也会观察到蛋白质水平的这种巨大差异。图7B中的GFP表达动力学显示出与图7A中生物量曲线相似的指数曲线,但分布范围更广。如前所述,GFP蛋白非常稳定。这在这里通过稳定期恒定的GFP荧光得到证明。其他蛋白质可能显示降解,并且经常暴露于蛋白水解。在这种情况下,生物量发展和蛋白质形成动力学的在线监测可以在早期生物工艺开发中提供有价值的信息。生成如此大量的在线信息需要进一步的数据分析。一个简单的分析示例是应用典型的评估标准,例如比产物产率(YP/X),它表示形成的产物与生物量的关系。
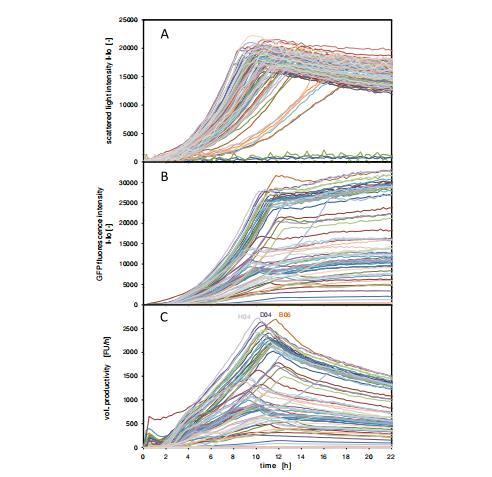
图7:克隆筛选-90个不同的多形汉逊酵母克隆的生长和GFP蛋白表达比较。(A) 通过散射光强度的生长;(B) 通过GFP荧光强度的蛋白质表达;(C) 体积生产率(Pv)- 计算为GFP形成速率,不考虑设备的设置时间,最佳克隆通过在图中给出孔号来描绘;45个多形汉逊酵母RB11-pC10-Mox-GFP克隆和45个多形汉逊酵母RB11-pC10-FMD-GFP克隆在缓冲YNB-G培养基中;在96孔MTP中测量,填充体积200μL,温度37°C,摇动频率995 rpm,摇动直径3 mm,散射光(激发:620 nm/发射:-,增益:20),GFP(激发:485 nm/发射:520 nm,增益:10)。
相关新闻推荐
1、疫苗候选菌株:猪胸膜肺炎放线杆菌生长曲线、溶血活性、 耐药性测定(四)
2、φR1-37噬菌体与小肠结肠炎耶尔森菌之间噬菌体-宿主相互作用的进程(三)
