各种不同的生态系统都存在微生物群落,典型的微生物群落包括土壤、海洋或江湖等环境微生物以及人体或动物肠道微生物等。其中,肠道微生物群越来越引起人类的重视,越来越多的证据表明人体肠道微生物群的组成和活性变化与多种疾病和生态表型有关,如糖尿病、肥胖、结肠炎和严重抑郁症等。
因此,若研究肠道微生物与宿主的关系,则能够更好地了解肠道共生体对疾病的作用机制,指导从肠道微生物角度出发的新的治疗方法和策略的构建,以达到治疗或预防疾病的目的。
近日,中国农业大学的团队和清华大学的团队在Microbiome上发表了名为“”的研究论文,开发基于液滴的微流控技术培养蜜蜂,验证了微流控液滴平台在肠道微生物培养组学中的可行性,为更复杂微生物群落的大规模研究铺平了道路。
一
传统培养方式限制测序技术深入研究微生物的基因型和表型多样性
复杂微生物群由多种微生物组成,这些微生物是多物种复合体的一部分。尽管属于同一属和种的微生物拥有一个共同的、且对于细胞功能和物种的生存至关重要的核心基因组,但它们仍然拥有相当数量的菌株特异性基因,导致它们在生理和毒性特性等方面的不同表型,这些差异菌株可能会在不同程度上改变肠道微生物群的功能,进而影响到宿主健康。
因此,表示,仅在物种水平上研究微生物群落是不够的,需要深入调查基因型和表型的多样性。培养是微生物研究的基础方法之一,但实际上由于培养条件的不适合,或是缺少互利共生的个体,很少有微生物可以在实验室条件下轻松培养,对于复杂群落而言,往往也只能成功实现其中一部分占多数的,或快速生长菌株的有效表征,并且传统的培养方式通常是低通量的,丰富的菌株多样性往往会在这个过程中被掩盖。
幸运的是,越来越强大的测序技术出现了,该技术可更深入、更清楚地了解共生肠道微生物组的结构、功能和多样性。16S rRNA基因测序(16S rRNA gene sequencing)和鸟枪法宏基因组测序(Shotgun metagenomic sequencing)是当前用于微生物群落分析的两种主要工具。
16S rRNA基因测序一般用于通过选择性扩增和测序微生物16S rRNA基因的高变区来识别和分类微生物,可以通过相对少量的原始读长来获得有代表性的细菌分类学估计。其具有高通量,成本低的特点,并拥有相当多成熟的生物信息学工具。但这种方法的主要限制为分类群是根据基因组的单个区域的序列分配的,这导致了分辨率不足。此外,扩增引物的选择也影响很大,一些引物已被证明会导致特定分类群的代表性过高或过低,这可能导致对分类单元的表示存在潜在偏差。
鸟枪法宏基因组测序对从整个微生物群落中分离出来的所有微生物的基因组进行测序。它的优势在于通过收集有关广泛基因组区域的序列信息,能够支持在物种水平上进行更准确的定义,提供更高的分类分辨率。同时还能支持进一步进行菌株水平的重建,得到新的基因或基因组,并对它们进行功能注释和途径预测以产生微生物群落的详细描述。但这种方法成本较高,需要深度测序获得更高的覆盖度以达到令人满意的分辨率,以及更复杂的下游分析。
“虽然基于测序的方法不限于可培养的微生物群,但16S rRNA基因测序方法在种内分析的分辨率上仍然极其有限,并且可能会被每个基因组的16S rRNA基因的多个不同拷贝混淆,这同样会造成对实际存在于环境中菌株功能的误判;鸟枪法宏基因组测序通过考虑更多标记基因或全基因组来提供更多信息,目前也已经开发了许多工具来分析宏基因组数据来解决这些问题,但来自取样时间的或空间的偏差往往需要更深的测序深度来弥补,但这也带来了急剧升高的成本。”说道。
二
液滴微流控平台可克服传统培养方式的缺陷
因此,若有一种培养方法可突破传统培养方式的局限,则会大大减轻测序技术的压力。基于液滴的微流控平台或许是个不错的选择。
液滴微流控
微流控(Microfluidics)是指一种在微米尺度空间对流体进行操控的技术,在该技术下可以将化学、生物等实验室的基本功能微缩到一个几平方厘米芯片上,因此又被称为“芯片实验室”。作为微流控芯片研究中的重要分支,液滴微流控是一种在微尺度的通道内利用流动剪切力或表面张力的改变,将两种互不相溶流体中的离散相流体分割成纳升级及以下体积的微液滴,并驱动微液滴运动对其进行操控的技术。
告诉生辉SynBio,基于液滴微流控的特征,我们可以通过在直径为数十至数百微米并由不混溶的油和工程表面活性剂分割的介质液滴种划分微生物来消除群落培养中过度生长的快速增长种群的影响。由于微制造的物理孔或通道不会限制液滴,因此可以快速创建数百万个独立的培养系统实现单个肠道微生物体的高通量培养。这极大克服了传统培养方式的缺陷,为通过培养来表征来自肠道共生体的稀有类群提供了机会。
为了证明微流控液滴平台在肠道微生物群研究中的可行性,和团队将蜜蜂作为研究对象。原因是与其他动物相比,蜜蜂的肠道细菌简单且稳定,宏基因组分析也表明,虽然蜜蜂肠道由数量有限的细菌系统发育型组成,但仍然存在显著的菌株水平多样性,个别菌株具有独特的基因组潜力和关键能力,这些能力在功能上与宿主的营养代谢和健康相关,为在菌株水平分析肠道共生体与宿主关系提供了很好的模型。
具体做法如下:首先,构建了一个微流体液滴平台,并产生了用蜜蜂肠道中的单个细菌细胞包裹的液滴;随后,收集液滴并进行孵育培养,确定了液滴中微生物的生长能力,宏基因组分析揭示了与常规测序方法相比蜜蜂肠道更高的菌株水平多样性,证明了微流体平台在分离和富集稀有微生物菌株方面的潜力。
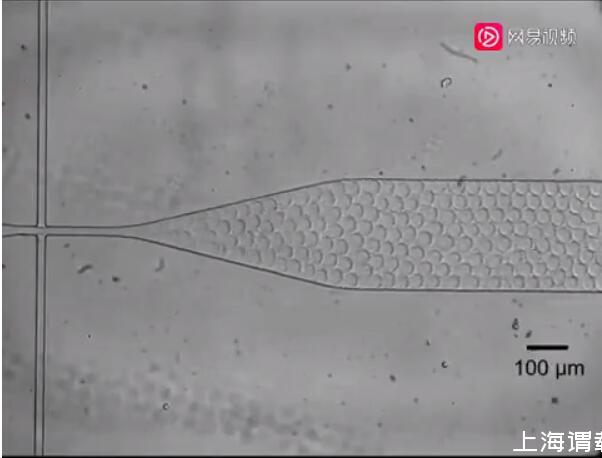
▲图丨微液滴生成(来源:郑浩)
最后,结合分箱策略,得到了蜜蜂肠道微生物的大量基因组草图,并进行了功能预测和比较基因组分析。对双歧杆菌属的分析揭示了潜在分类单元的存在,它们在跨膜运输、肌醇利用以及多糖利用方面存在丰富的菌株多样性。研究人员还得到了来自Lactobacillus panisapium的新菌株,该菌种在以往的研究中被认为特异性来源于中华蜜蜂;通过进一步的基因组比较,发现来自西方蜜蜂的菌株中独特地含有一组与饮食阿拉伯糖利用相关的代谢基因簇,包括araf43A,rafB,abfA和abfB,这可能与它对不同蜜蜂宿主的适应密切相关。
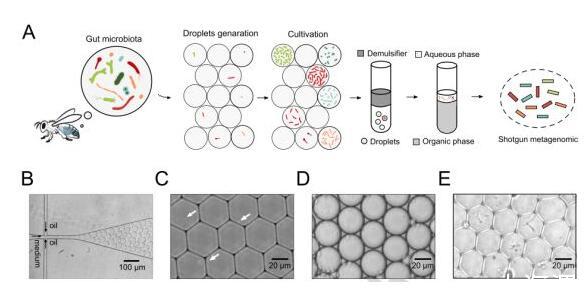
▲图丨微流控液滴中蜜蜂肠道细菌的单细胞封装和培养(来源:研究论文)
“总体而言,结果证明了基于液滴的培养在研究蜜蜂肠道微生物多样性方面的适应性,同时这种方法也有潜力适用于其他复杂群落,在稀有类群的获得以及功能鉴定方面发挥作用。”说道。
他补充道,对于肠道微生物,当前的研究主要集中在特定培养基质下的微流体液滴培养,结合16s rRNA扩增子测序以研究肠道微生物个体的膳食碳水化合物代谢或抗生素耐药性。我们的研究则着重于通过隔离培养以富集在常规状态下难以检测的稀有类群,结合宏基因组的测序和分析,以较高通量实现对肠道稀有微生物的发现,以及代谢途径和功能预测,提供关于宿主和肠道共生体关系的崭新理解。
“未来,我们可能会通过调整液滴大小、改善培养条件和测序方法来研究肠道真核微生物,并实现对单胞的高通量识别,这将进一步扩大我们对肠道复杂成员的理解。同时,我们的流程也可以进一步应用于人类肠道共生体的研究,扩展对人类肠道稀有类群以及它们与健康关系的认知和了解。”
参考资料:
1.https://blog.csdn.net/woodcorpse/article/details/125118043
相关新闻推荐
3、北极狐唾液乳杆菌ZJBF005生长曲线、产酸和耐酸曲线、抗菌活性测定(三)
