凉粉草是一种传统药食两用植物,生长于中国东南部、东南亚和印度东北部。因其在中国古代民间医学中享有盛誉,可治疗多种疾病,因此也被称为“神草”。根据中药药典,凉粉草天然富含生物活性多糖和多酚,可用于治疗中暑,保护肝功能。凉粉草多糖(MCP)是一种棕色酸性阴离子杂多糖,主要由半乳糖、葡萄糖、甘露糖和半乳糖醛酸组成。由于天然结合的棕色生物活性物质(例如多酚和有机酸),这些多糖呈现棕色。MCP与这些生物活性化合物的组合,称为MCP复合材料(MCPC),表现出许多健康益处。
MCPC的研究主要集中在宏观水凝胶,而不是微米或纳米凝胶。然而微型水凝胶(微凝胶)比宏观水凝胶具有更可控的吸收和响应释放特性。对肠-肝轴的研究表明,口服益生菌参与库普弗细胞调节、内毒素易位和肠源性代谢物迁移,有助于在肝损伤中发挥保肝作用。益生菌Akkermansia muciniphila(AKK)通过调节肠道菌群的组成和代谢功能并激活磷脂酰肌醇3-激酶(PI3K)/Akt通路,从而改善药物引起的氧化性肝损伤。活的AKK或双歧杆菌比巴氏灭菌形式对肝损伤具有更强的抗炎和抗纤维化作用。
益生菌在加工、储存和胃肠道条件下面临着严峻的挑战。具有pH响应性的多糖基微凝胶可以保护益生菌免受刺激性胃酸的侵害,并以可行的形式在肠道中响应性地释放它们。多糖水凝胶是半固体且机械强度较弱。通常需要额外的交联,例如二硫键来固化水凝胶。然而将益生菌封装在机械强度较高的载体系统内非常重要。如果壁材多糖同时能够被肠道菌群用作益生元,那就更有利了。
在这项研究中,我们开发了一种具有肠道反应性和粘膜粘附特性的铁离子交联MCP微凝胶,并通过自然结合的棕色生物活性物质的酚醛金属骨架进行机械强化。这些微凝胶在酸性条件下具有完整的结构,并且仅在pH中性条件下破裂,可以响应地释放具有高粘膜粘附和定殖的高活性益生菌。棕色生物活性物质通过疏水相互作用和氢键与多糖(MCPC)天然结合,并表现出出色的抗炎和抗氧化特性。这些棕色生物活性物质是精确的益生元,可以特异性提高体内阿克曼氏菌属的丰度。然后,将益生菌Akkermansia muciniphila(AKK)装入棕色生物活性框架强化微凝胶中。与游离AKK和巴氏灭菌AKK相比,MCPC成分和负载AKK之间具有更强的协同健康益处。
MCPC微凝胶可以专门向肠道输送高活性AKK,从而调节微生物群平衡并保护肠道屏障。MCPC微凝胶还将抗氧化棕色生物活性物质专门输送到肝脏中,以减轻肝脏氧化应激和炎症。
Bioscreen全自动生长曲线分析仪的应用
将初始益生菌密度为10 6 CFU mL−1的MCPC/NZ9000在MRS培养基(pH 5.5)中培养,使用CLSM监测益生菌的生长。通过Bioscreen C自动生长曲线分析仪在OD 600 nm处监测MCPC/WCFS1的生长。每1小时获取OD 600值,共80小时。
实验结果
成功制备了机械强度高的MCPC微凝胶,该微凝胶通过酚类金属配位框架稳定,用于益生菌和多酚的共同递送。该微凝胶具有增强的益生菌胃酸保护、肠道响应释放和粘膜粘附特性的组合。棕色生物活性物质天然结合在MCP多糖上,事实证明,MCP多糖是提高阿克曼氏菌丰度的精确益生元。MCPC/AKK通过依次在肠道中提供活性AKK并在肝脏中提供棕色抗氧化剂,有效改善APAP诱导的肝损伤。MCPC微凝胶在肠道中的高活性AKK可以恢复肠道微生物失调并促进SCFA产生,从而增强肝功能,调节氧化应激和炎症,并通过肠肝轴修复肠道屏障。
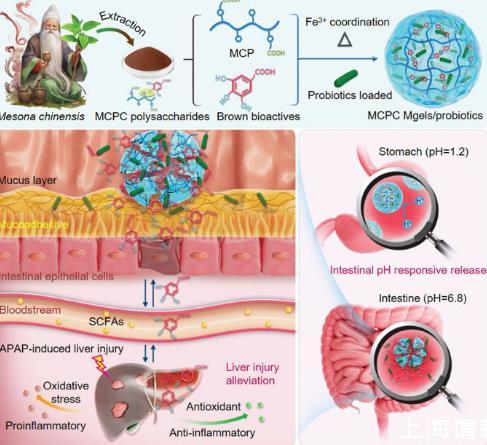
图1、酚醛金属配位框架稳定的凉粉草多糖复合物(MCPC)微凝胶,用于控制释放对乙酰氨基酚(APAP)诱导的肝损伤。采用MCP和棕色生物活性物质组成的MCPC,通过离子配位制备微凝胶。微凝胶内的棕色生物活性物质-Fe 3+酚醛金属骨架为微凝胶提供了机械结构支撑。MCPC微凝胶表现出胃酸耐受性,有利于益生菌保护,并根据肠道pH值释放益生菌。这有助于益生菌粘附、保留和定植于肠道。当微凝胶解离时,棕色生物活性物质依次释放,吸附的半乳糖片段通过肝细胞半乳糖受体的识别,促进生物活性物质进入肝脏。肠道中释放的益生菌和肝脏中的棕色生物活性物质的协同作用有助于减轻APAP引起的小鼠肝损伤。
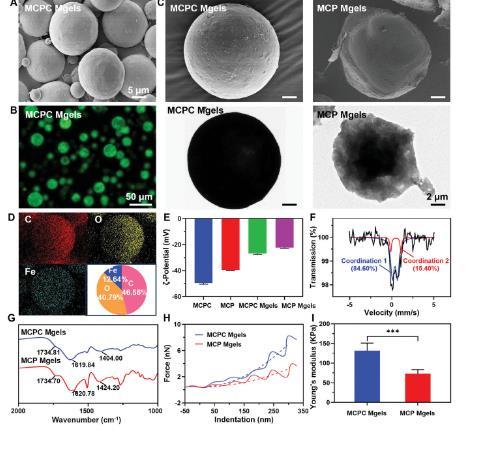
图2、MCPC和MCP微凝胶的制备和表征。A)MCPC微凝胶的SEM。B)用罗丹明B染色的MCPC微凝胶的光学显微镜图像。C)MCP和MCPC微凝胶的SEM和TEM。D)MCPC微凝胶的元素图谱。E)MCPC、MCP及其微凝胶的z-电位。F)MCP微凝胶的穆斯堡尔谱。G)MCPC和MCP微凝胶的FT-IR光谱。H)纳米压痕力-距离曲线,I)MCPC和MCP微凝胶的杨氏模量。
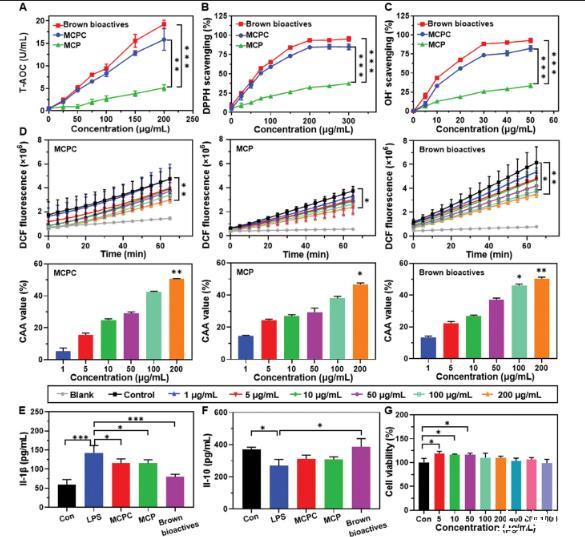
图3、评估MCPC、MCP和棕色生物活性物质的体外抗氧化、抗炎和细胞毒性特性。A)总抗氧化能力(T-AOC),B)DPPH自由基,C)MCPC、MCP和棕色生物活性物质的羟基自由基清除能力。D)MCPC、MCP和棕色生物活性物质的细胞抗氧化活性。使用MCPC、MCP和棕色生物活性物质进行酶联免疫吸附测定(ELISA),以检查E)IL-1β和F)IL-10的水平。原始246.7细胞用MCPC、MCP和棕色生物活性物质(200µg mL−1)预处理24小时。G)MCPC对Caco-2细胞的细胞毒性评估。
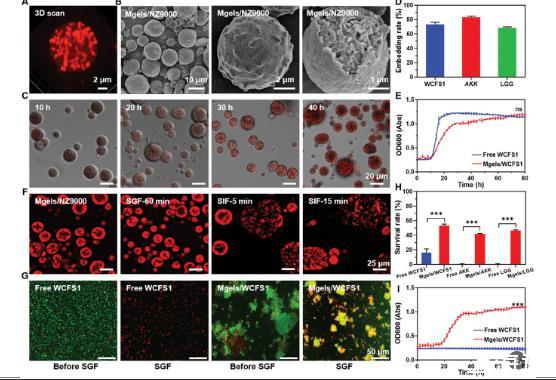
图4、pH响应型MCPC微凝胶可实现肠道响应性释放并增强益生菌的活力。A)CLSM和B)加载NZ9000(红色)的MCPC微凝胶的SEM图像。C)CLSM图像显示NZ9000在M17肉汤(pH 5.5)中的微凝胶中生长。D)微凝胶对各种益生菌的包封效率。E)Bioscreen C全自动生长曲线分析仪测试MRS肉汤中游离WCFS1和MCPC/WCFS1的生长曲线(80h)。F)MCPC/NZ9000微凝胶在SGIF中处理前后的荧光图像。G)活细胞(绿色)/死细胞(红色)活力,H)存活计数,I)Bioscreen C全自动生长曲线分析仪测试游离WCFS1和MCPC/WCFS1在SGF处理前和处理30分钟后的对应的生长曲线((80h))。
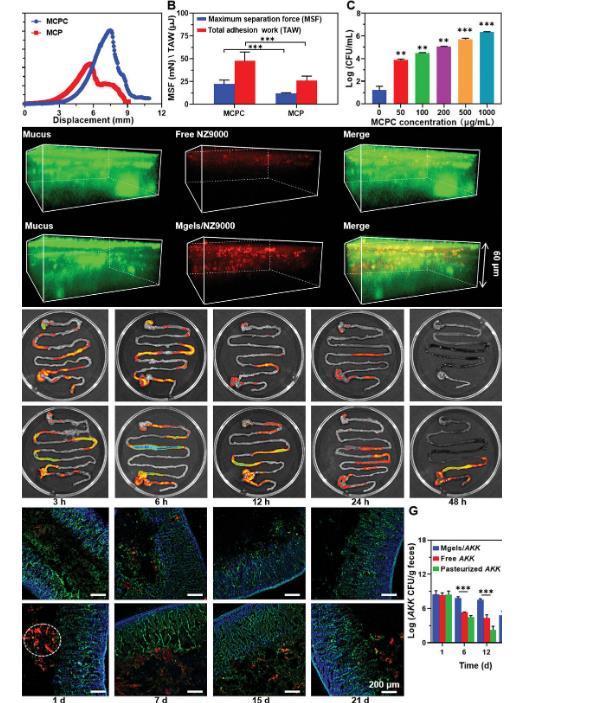
图5、通过与MCPC介导的相互作用增强肠道粘膜粘附和益生菌定植。A)粘膜粘附曲线,B)MCPC和MCP对大鼠肠粘膜的最大分离力(MSF)和总粘附功(TAW)。C)MCPC浓度对粘液粘附益生菌影响的菌落计数。D)粘液(用绿色Alexa Fluor 488-WGA标记)渗透无红色和嵌入NZ9000的CLSM 3D图像。E)FITC标记的游离WCFS1或MCPC/WCFS1在胃肠道中的滞留。F)红色游离NZ9000或MCPC/NZ9000在肠粘液中的分布。空肠粘液用绿色Alexa Fluor 488-WGA染色,肠绒毛细胞核用蓝色DAPI染色。G)小鼠粪便中各种AKK的菌落计数。
总结
口服益生菌在加工、储存和胃肠道恶劣条件下面临挑战。基于多糖的水凝胶递送系统在益生菌保护方面很有前景,但其半固体且强度较弱,并且往往需要额外的交联来固化其结构。研究人员开发了一种具有肠道反应性和粘膜粘附特性的铁离子交联MCPC微凝胶。首先将MCPC分离为MCP和棕色生物活性物质,并研究了它们的化学成分。然后比较了Fe3+交联MCPC和MCP微凝胶的理化性能,尤其是机械强度。研究了负载益生菌的MCPC微凝胶的胃酸耐受性、肠道pH响应性和粘附保留特性。微凝胶成分的益生元作用也在体内进行了评估。最后,研究了其对急性肝损伤小鼠模型的缓解作用,重点关注氧化应激、炎症和肠道菌群调节。这项研究为应用MCPC微凝胶益生菌递送系统通过肠-肝轴缓解肝脏疾病提供了灵感,提供了一个强大的基于天然多糖的微凝胶平台,用于通过肠肝轴控制释放和靶向输送具有健康潜力的益生菌。
相关新闻推荐
1、禽呼肠病毒S1133毒株接种DF1细胞一步生长曲线的绘制——材料与方法
3、EcSF工具预测发酵生肉香肠加工和储存过程中产志贺毒素大肠杆菌的浓度(一)
