Bioscreen生长速率测定
为了进行生长速率测定,菌株首先在酵母提取物蛋白胨葡萄糖培养基中预生长至早期稳定期。用冰冷无菌水洗涤沉淀后,将细胞接种到200微升含有20克/升葡萄糖的合成培养基中,初始OD600值为0.1。滴定板在Bioscreen C微生物生长曲线分析仪(Labsystems)中35°C连续振荡孵育,每30分钟监测OD600值。
细胞质量和代谢物浓度的分析
接种到发酵培养基中的细胞干重(DW)基于光密度(OD600纳米)估算。干重首先通过将已知OD600值的10毫升培养物等分试样过滤到预称重的0.2毫米Supor膜盘滤器(PALL Corporation,美国)上,用MilliQ水洗涤滤器,并在微波炉中以约150瓦干燥15-20分钟至恒重来测量。确定每个测试菌株的干重与OD600值之间的相关性。
发酵实验样品中的代谢物和底物通过Waters等度Breeze HPLC系统(Waters,美国马萨诸塞州米尔福德)使用离子交换柱WAT010290和折射率检测系统(Waters 2414 RI检测器)进行分析。柱温维持在75°C,使用5 mM H2SO4作为洗脱液,流速为1毫升/分钟。对于水解物培养基的分析,样品首先在15毫升离心管中以4000克离心10分钟。上清液进一步在2毫升微量离心管中以20,000克离心5分钟,然后使用0.2微米滤器过滤。滤液用于高效液相色谱HPLC分析。超高浓度发酵中的乙醇通过近红外光谱法(Alcolyzer,Anton Paar)测量。速率和产量按此前描述的方法计算。
结果
酿酒酵母菌株库的抑制剂耐受性筛选
我们首先旨在获得在富含抑制剂的木质纤维素水解物中直接生长和发酵性能极高的菌株,因为对多种抑制剂的同时耐受性对于木质纤维素水解物中的高生产力很重要。为此,使用未脱毒的酸预处理云杉水解物作为筛选培养基,因为这种水解物比大多数其他水解物含有更多且浓度更高的抑制剂。使用这种培养基,我们首先筛选了580种不同的酿酒酵母菌株在不同浓度的云杉水解物中生长的能力。菌株库由实验室菌株、工业菌株(葡萄酒、啤酒、面包和生物乙醇生产菌株)以及各种来源的天然分离株组成。第一次筛选是在含有高达70%云杉水解物全浆液(pH 5.5)的YP琼脂平板上进行生长测试。
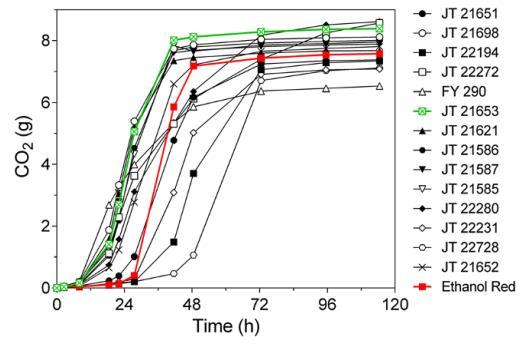
图1 14种不同预选抑制剂耐受性酵母菌株与Ethanol Red的发酵性能比较。半厌氧发酵在含有30%预处理云杉水解物浆液并补充YP和葡萄糖至200克/升、pH 5.5的条件下进行。发酵过程通过发酵过程中CO2产生导致的重量损失来跟踪。强健的工业菌株Ethanol Red(红色)用作参考,菌株JT21653(绿色)被选为表现最佳的菌株。
从测试的580个菌株中,随后在30%云杉水解物(补充YP和葡萄糖至200克/升,pH 5.5)中通过测定其发酵性能对平板测试中表现最好的35个菌株进行了更详细的筛选。使用高浓度葡萄糖是为了在发酵开始时获得高渗透胁迫,在结束时获得高乙醇胁迫。工业菌株Ethanol Red用作对照。在测试的35个菌株中,我们选择了14个至少显示出与工业菌株Ethanol Red相似发酵性能的菌株。最后,在单一发酵实验中再次测试了14个最佳菌株的发酵性能,发现10个菌株的表现始终优于Ethanol Red。它们主要表现出更短的迟滞期。表现最佳的菌株JT21653既表现出更短的迟滞期,又表现出更完全的糖衰减,因此被选择用于进一步分析。JT21653是从当地商业来源购买的面包酵母。在BCCM/MUCL(鲁汶天主教大学真菌库,比利时新鲁汶)对单细胞分离株进行了物种鉴定测试,确认该酵母为酿酒酵母 Meyen ex. E.C. Hansen。DNA含量的流式细胞术分析显示JT21653具有三倍体基因组。该菌株表现出良好的孢子形成和高孢子活力,因此被选择用于进一步分析。
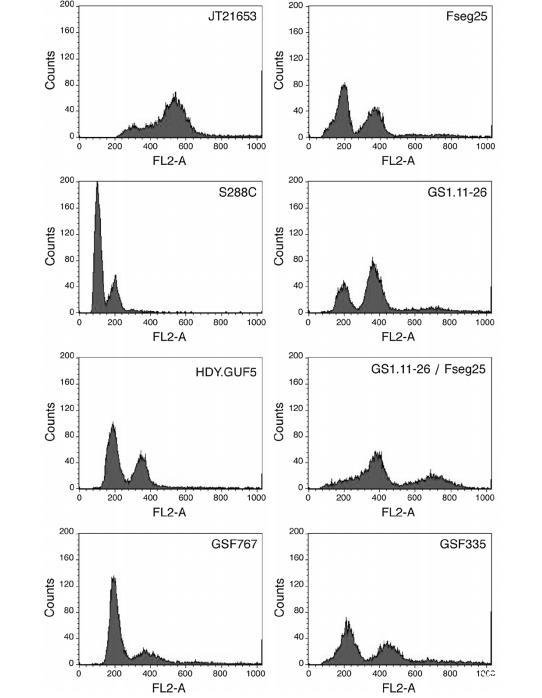
图2 通过流式细胞术测定DNA含量。菌株生长至指数期,然后用乙醇固定,DNA用碘化丙啶染色。使用对照单倍体(S288c)和二倍体(HDY.GUF5)菌株。
JT21653抑制剂耐受性分离株的分离
为了选择抑制剂耐受性至少与三倍体亲本一样好的JT21653分离株,我们筛选了41个JT21653分离株在40%云杉水解物(补充YP和葡萄糖至200克/升,pH 5.5)下半厌氧条件下的发酵性能。从这次预筛选中,我们选择了15个发酵性能最佳的分离株。为了选择最具抑制剂耐受性的分离株,将云杉水解物的浓度提高到77%并补充70克/升葡萄糖。这种浓度的云杉水解物对工业菌株Ethanol Red、三倍体亲本JT21653以及15个分离株中的大多数具有严重抑制作用,而四个分离株能够在这些条件下完成发酵,尽管速率不同。一个名为Fseg25的分离株表现异常出色,以几乎没有迟滞期开始发酵,并在大约48小时内完成,此时其他分离株中只有另一个刚刚开始发酵。Fseg25的DNA含量流式细胞术分析表明该菌株具有二倍体基因组。此外,它能够与MATα/α菌株交配,表明它是MATa/a,并且产生的四倍体菌株产生了有活力的孢子。因此,选择Fseg25分离株作为与二倍体MATα/α菌株GS1.11-26遗传重组的交配伙伴。
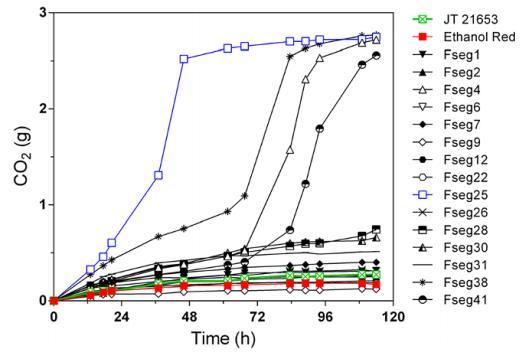
图3 从抑制剂耐受性面包酵母JT21653中选择优良分离株。发酵在半厌氧条件下使用77%浓度的云杉材料处理浆液并补充70克/升葡萄糖进行。CO2产生从重量损失估算。Fseg25(蓝色)表现最佳,特别是与其他分离株相比迟滞期非常短。二倍体亲本JT21653(绿色)和工业生物乙醇生产菌株Ethanol Red(红色)以及除四个以外的所有其他分离株,在120小时内无法在这种浓度的云杉水解物中显著发酵。
GS1.11-26与Fseg25的减数分裂重组
为了将GS1.11-26的优良D-木糖发酵性能与Fseg25的优良抑制剂耐受性状结合起来,我们将MATα/α菌株GS1.11-26与MATa/a分离株Fseg25交配。产生的四倍体菌株进行孢子形成,筛选819个减数分裂分离株,以选择具有所需特性的二倍体杂交F1分离株,主要是高效的D-木糖发酵、快速有氧生长和高抑制剂耐受性。
