摘要
理解大肠杆菌在不同微生物组成的土壤中的存活和持久性,对于水质评估和微生物源追踪的准确性至关重要。本研究通过微宇宙实验,调查了三种大肠杆菌菌株(分别来源于土壤、狗粪便和人粪便)在微生物群落组成改变土壤中的存活模式。将浓度递增的3号胆盐(0.05%、0.15%、0.30%和0.50%)加入砂壤土中,孵育90天。然后将实验室培养的大肠杆菌接种到土壤中,再孵育150天以监测其存活模式。通过培养法和培养非依赖法(PCR-变性梯度凝胶电泳)检测胆盐对细菌群落多样性的改变。总体而言,胆盐浓度的递增导致10天和90天孵育时的菌落形成单位计数均下降。DGGE分析表明,细菌群落在10天时仅有轻微变化,但在90天时发生显著变化。聚类分析显示胆盐处理组与对照组分开聚类。大肠杆菌在土壤中的存活受微生物群落复杂度的显著影响,随着微生物群落多样性的降低,大肠杆菌的死亡速率逐渐下降。不同土壤微生物压力下大肠杆菌的差异存活强调了在水质管理和微生物源追踪预测模型中纳入生物因素的重要性。
1. 引言
为降低环境水体中污水传播病原体的感染风险,美国环保署和世界卫生组织基于粪便指示菌的浓度制定了水质标准,因为这些指示菌通常比肠道病原体数量更多,因而更容易检测。指示菌(如大肠杆菌)被用作粪便污染的信号,基于以下假设:环境中大肠杆菌的唯一重要来源是人和温血动物的粪便;大肠杆菌与病原菌株具有相似的存活模式;一旦从宿主排出,它们不会在环境中繁殖。然而,热带和温带地区的多项近期研究表明,在适宜的外部环境条件下,大肠杆菌可以繁殖并达到高密度,这削弱了其作为粪便污染指示菌的适用性。因此,深入理解大肠杆菌对各种环境因子的响应对流域管理和监管标准至关重要。
土壤是大肠杆菌进入水体的主要非点源。农业来源的大肠杆菌通过施用动物粪肥或放牧牲畜的直接沉积进入土壤。土壤结合的大肠杆菌通过雨水/径流进入水体系统,从而影响水中大肠杆菌的水平。考虑到对周边水体的污染风险,大肠杆菌在土壤中的存活/持久性是一个关键问题,但由于缺乏有关土壤因子影响的信息,这一问题尚未得到明确界定。非生物因素如温度、水分、土壤质地、有机质含量和粪肥介质已被证明影响大肠杆菌在土壤中的存活,尽管这些因素如何影响大肠杆菌尚不清楚。一些生物因素如捕食作用也被报道影响大肠杆菌在土壤中的持久性。然而,对其他生物因素(如土壤微生物群落组成)影响的理解仍然非常有限。
研究表明,微生物引入土壤后的存活或持久性受土著土壤微生物群落结构的控制。研究发现铜绿假单胞菌的存活率与小麦根际微生物多样性的复杂度呈负相关。在另一项人工构建微宇宙的研究中,青枯雷尔氏菌生物型2的入侵能力与土壤微生物群落多样性的程度呈负相关。Van Elsas等证明,大肠杆菌O157:H7的存活受土壤微生物群落复杂度的负面影响。大肠杆菌物种具有遗传多样性,研究表明致病性菌株与非致病性菌株的存活方式不同。因此,将致病性菌株的环境行为推广到其他大肠杆菌群体是不恰当的。
作为选择性抑制剂,3号胆盐广泛用于微生物培养基,浓度为0.15%,以支持革兰氏阴性肠道细菌的生长。BS3已被用于土壤微宇宙研究以降低土著土壤细菌数量,从而促进天然大肠杆菌种群的生长。在本研究中,BS3用于构建具有微生物群落结构梯度的土壤微宇宙,这些微宇宙被用作具有不同微生物群落结构的模型土壤生态系统,以确定接种大肠杆菌菌株的存活情况。假设以不同浓度向土壤施用BS3将导致土壤微生物群落组成逐渐改变,这将反向影响接种大肠杆菌的存活。
2. 材料与方法
本研究使用的实验方案总结如图1所示。实验设置的详细描述如下:
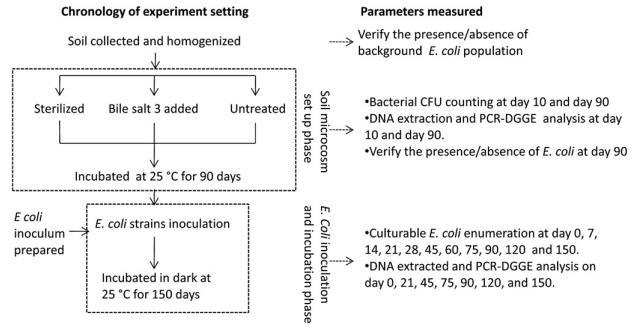
2.1 土壤采样与处理
砂质土壤新鲜采集自佛罗里达州皮尔斯堡印第安河研究与教育中心草地表层10厘米。该草地由柑橘园改造而来已有10年,改造后未施用有机改良剂。去除所有石块和植物残体后,土壤用2毫米筛网均质化,储存于4°C并在10天内用于设置土壤微宇宙。部分土壤按照Unc和Goss的程序,在121°C下连续5天每天高压灭菌2小时进行灭菌。为便于孢子萌发,高压灭菌间隔期间将土壤样品在无菌条件下室温保存。蒸发损失的水分通过向土壤添加相应量的无菌去离子水进行补偿。将高压灭菌土壤的等分试样平板稀释涂布于营养琼脂平板,室温培养48小时以检查高压灭菌效果。48小时后未检测到生长。
通过以下方法验证采集土壤中背景大肠杆菌种群的存在/缺失:将1克均质土壤悬浮于10毫升胰蛋白胨大豆肉汤中,振荡并在37°C下孵育24小时(三次重复)。将200微升增菌培养物涂布于mFC琼脂平板(两次重复),35°C孵育2小时,然后在44.5°C下孵育22小时。未观察到蓝色菌落,表明接种前土壤样品中不存在背景大肠杆菌。
2.2 土壤微宇宙设置
将新鲜土壤放入灭菌容器中。将20%胆盐溶液喷入土壤并均质化,最终浓度为0.50%、0.30%、0.15%或0.05%。未添加BS3的新鲜土壤和灭菌土壤分别用作阳性和阴性对照。土壤水分含量用灭菌去离子水调整至田间持水量的50%,将100克土壤放入用封口膜覆盖的玻璃瓶中,在25°C黑暗条件下孵育总计90天,以建立一系列微生物群落结构逐渐改变的土壤生态系统。共建立594个微宇宙(6种处理 × 3种大肠杆菌菌株 × 接种后11次破坏性采样事件 × 每次3个重复)。每5天评估所有核心的水分含量,并以滴加形式添加损失的水量(无菌蒸馏水),以保持处理内恒定的水分状态。在10天和90天时对微宇宙进行采样,使用培养法和非培养法监测微生物群落的变化。使用上述方法检测90天时大肠杆菌的存在/缺失。此时未检测到大肠杆菌生长。90天孵育的土壤微宇宙用作大肠杆菌接种的受体。
相关新闻推荐
1、结核分枝杆菌通过分泌D-丝氨酸抑制T细胞功能实现免疫逃逸(一)
2、海洋来源氨基香豆素增强多粘菌素B抗伯克霍尔德菌活性(一)
