从附录图4可以看出,毒物兴奋效应在18到24小时间逐渐增强,最大刺激从39%增加到74%。此外,当SM浓度超过2.24x10⁻⁵ mol/L(LogC: -4.65)时,抑制效应进一步增强。根据费氏弧菌的生长曲线(图2),生物发光的下降和细菌密度的稳定表明C6的浓度下降,而C8的浓度保持稳定。此时,低剂量SM可能进入细胞质并激活LuxR蛋白的表达,使C8与LuxR结合以增加生物发光。
其他SAs在Dhps中的对接结果见附录图3,并观察到类似的受体-配体相互作用。结果表明SAs可以竞争性地结合Dhps并减少Dhps-PABA复合物的数量。另外五种SAs(SDX, SMX, SPY, SCP, SMR)在0到24小时内对费氏弧菌生物发光的毒物兴奋效应如附录图5-9所示;它们表现出与SM相似的行为,表明SAs对费氏弧菌的时间依赖性毒物兴奋效应是这些药物的共同属性。
3.3. B3O对费氏弧菌的时间依赖性毒物兴奋效应
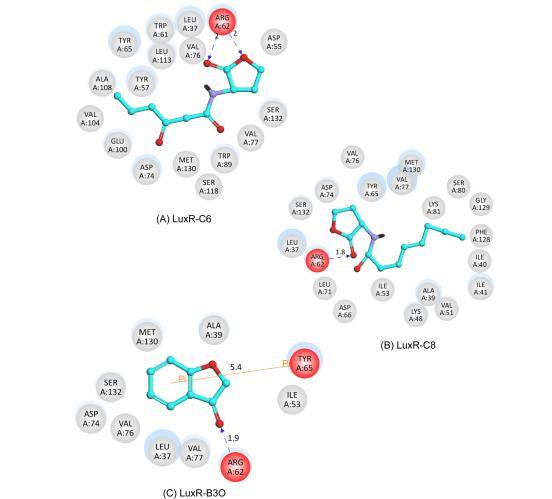
图5. C6(A)、C8(B)及B3O(C)与LuxR蛋白对接时的配体相互作用示意图。蓝色虚线与黄色实线分别表示配体与氨基酸残基之间的氢键及π-π键。
附录图4(B)显示了B3O在0到24小时内对费氏弧菌生物发光的个体效应。此效应可分为四个阶段,图3(B)显示了B3O在0、4、10、18和24小时对费氏弧菌的毒物兴奋效应。第一阶段从0到2小时,其特征是随着B3O的添加,抑制效应增加。由于呋喃酮B3O和C6信号分子具有相似的脂溶性和水溶性,它们在LuxR中具有相同的结合位点,这些分子的对接视图如图5所示。可以看出,两个氢...LuxR-B3O > LuxR-C6。B3O能够快速进入细胞并与LuxR蛋白的残基结合(图5A);然而,对于B3O(图5C),除了氢键外,B3O的苯环和Tyr-65残基之间还存在pi-pi相互作用。这些观察结果为受体-配体稳定性顺序提供了证据:LuxR-B3O > LuxR-C6。B3O能够快速进入细胞,并通过竞争性地结合LuxR蛋白从而破坏费氏弧菌中luxICDABEG基因的表达,导致抑制作用。
时间依赖性毒物兴奋效应的第二阶段发生在3到6小时间,并表现出明显的毒物兴奋效应。引起刺激所需的浓度相对较低,效果范围从2.23x10⁻⁴ 到 9.63x10⁻⁴ mol/L(LogC:从-3.65到-3.02),在5小时时最大刺激达到254.18%。根据费氏弧菌的生长曲线,HV值持续下降而OD值逐渐增加,这表明C6和LuxR蛋白浓度低,而C8和AinR浓度高。分子对接可用于解释此期间的强烈刺激。C8和B3O在LuxR蛋白结合位点的对接视图如图5所示。可以看出,C8和ARG-62残基之间只形成一个氢键(图5B)。对于B3O(图5C),除了氢键外,B3O的苯环和Tyr-65残基之间还形成了另一个pi-pi相互作用,这使得可以确定受体-配体稳定性顺序:LuxR-B3O > LuxR-C8。类似地,我们推测复合物稳定性顺序如下:AinR-B3O > AinR-C8。在渗透到细菌内后,B3O首先与AinR蛋白结合。然后,C8可以与LuxR结合形成LuxR-C8复合物,该复合物编码发光基因的正调节因子并促进发光。高浓度B3O引起的抑制是由于多余的B3O与LuxR结合的结果。
第三阶段(7-16小时)的特点是,当存在低浓度B3O时,刺激效应几乎消失,并且随着暴露时间的增加,抑制效应减弱。当费氏弧菌的生长进入指数期时,C6、C8、LuxR和AinS的浓度急剧增加。由于B3O首先与AinR结合,然后与LuxR结合,由于AinR数量的增加,B3O在低浓度下产生还原性抑制效应。当B3O浓度高时,它可以完全结合AinR,剩余部分将与LuxR相互作用以抑制生物发光。
第四阶段包括从17到24小时的暴露时间,在附录图4(B)中可以观察到明显的时间依赖性毒物兴奋效应。B3O对生物发光的刺激作用随着暴露时间的增加而增强。具体而言,在17小时时,刺激浓度范围从2.23x10⁻⁴ 到 6.04x10⁻⁴ mol/L(LogC:从-3.65到-3.22),在24小时时,从2.23x10⁻⁴ 到 9.63x10⁻⁴ mol/L(LogC:从-3.65到-3.02),最大刺激从44.40%增加到153.85%。在此期间,细菌生长进入稳定期,生物发光开始下降。相反,OD值继续增加。此时,C6浓度下降,而LuxR和AinR蛋白均大量表达。因此,毒物兴奋效应的机制类似于第二阶段(3-6小时)发生的机制。
相关新闻推荐
1、解锁微生物代谢奥秘:新一代生长曲线分析平台加速乳糖/纤维二糖代谢研究(三)
