2.3. 费氏弧菌的生长曲线测试
采用96孔微孔板法测定费氏弧菌的生长曲线。该测定使用白色不透明96孔微孔板测定生物发光曲线,使用透明96孔微孔板测定细菌生长曲线。将细菌(T3突变体)从琼脂斜面接种到液体培养基中。生物发光和光密度分别在20°C下,使用Luminoskan Ascent Thermo Scientific化学发光分析仪和Bioscreen C MBC自动生长曲线分析仪每0小时测定一次,持续24小时。
2.4. 时间依赖性毒性测试
通过96孔微孔板法进行QSI和六种SAs的时间依赖性毒性测试。化学品浓度系列在板上以三重复分布。每孔含有80μL化合物或2%氯化钠溶液(作为对照)、80μL培养基和40μL制备好的费氏弧菌。使用Luminoskan Ascent Thermo Scientific化学发光分析仪在20°C下,每隔1小时测定费氏弧菌的相对发光单位,持续24小时。毒性结果以抑制率表示如下:
抑制率 = (RLU0 - RLU) / RLU0 × 100%
其中,RLU0是费氏弧菌暴露于对照的平均RLU值,RLU指暴露于测试化学品的平均RLU值(三次实验)。
在研究单一化学品的24小时毒性后,基于RLU的抑制率,使用概率单位模型计算中位效应浓度。根据EC50,获得了具有等毒比(相同的EC50值)的QSI和六种SAs的一系列二元混合物。测试采用与个体毒性测试相同的方法进行。
2.5. 同源建模和分子对接
使用Discovery Studio 3.1中的MODELER对LuxR进行同源建模。来自费氏弧菌的AAQ90196被选为本研究的目标LuxR蛋白。通过使用DS中实现的BLAST模块扫描NCBI的蛋白质数据库来准备模板。详细信息见支持信息。
分子对接基于DS,使用默认参数的CDOCKER协议进行。分子对接中使用的化学品(配体)的三维结构用Chemoffice生成,对接前使用CHARMm力场对配体进行能量最小化。基于CDOCKER,选择给出最低相互作用能的底物方向进行对接后分析,并利用产生最低对接能量的结合情况进行进一步分析。
二氢蝶酸合酶(Dhps)的建模和对接研究采用类似方法进行。选择TP-203863作为目标序列,1AJ0作为Dhps建模的模板。更详细的信息见支持信息。
3. 结果与讨论
3.1. 费氏弧菌的生长曲线
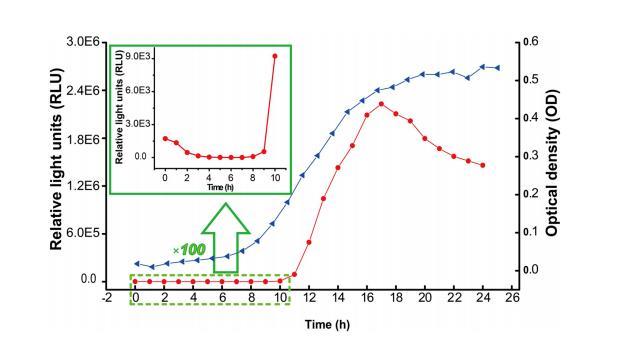
图2 蓝线和红线分别表示费氏弧菌在24小时内的生物发光(HV)和生长(OD)曲线。
如图2所示,费氏弧菌(HV)的生物发光在0到10小时之间较弱,在17小时迅速增加到峰值,然后逐渐下降。上述行为密度依赖于并受群体感应系统控制。费氏弧菌的生长曲线(OD)显示在延迟期(0-8小时)细菌密度较低,在此期间细胞产生并释放低浓度的N-(3-氧代己酰)高丝氨酸内酯信号分子(C6)以及LuxR蛋白。在6小时,N-辛酰HSL信号分子(C8)正在增加;这些分子可以与AinR结合,通过增加LuxR蛋白的量来加速细菌的生长。因此,C8有机会与LuxR结合,促进luxICDABEG的表达。图2中的插图显示,8小时后细菌生长进入指数期,细菌密度急剧上升,C6和LuxR增加,导致发光强度迅速增加。发光从17小时到24小时的下降表明C6开始减少,尽管C8的浓度仍然很高,因为细菌数量在稳定期缓慢增加。
3.2. SAs对费氏弧菌的时间依赖性毒物兴奋效应
测定了SAs对费氏弧菌在24小时内每小时的毒性效应,SM的时间依赖性结果见附录图4。简而言之,图3(A)显示了SM在0、4、10、18和24小时对费氏弧菌的毒物兴奋效应。在0到3小时间,没有观察到对生物发光的刺激或抑制,因为当培养条件改变时,细菌的生长受到许多影响因素的抑制。作为因素之一,外源化学品对费氏弧菌的生物发光影响轻微。
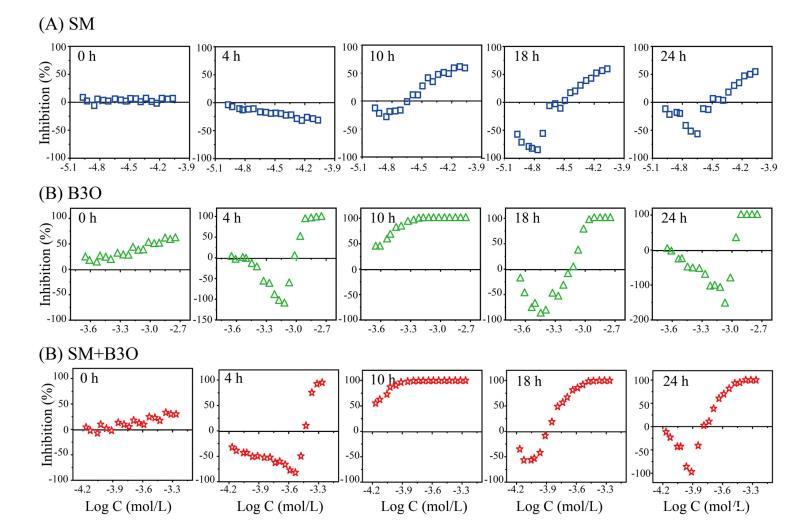
图3. SM、B3O及其混合物对费氏弧菌(V. fischeri)在0、4、10、18及24小时内的毒性作用。(A) SM;(B) B3O;(C) SM与B3O联用。
当暴露时间从4小时增加到8小时时,在附录图4中仅能观察到刺激作用,并且这种刺激与SM的浓度具有剂量-反应关系。此时,细菌中LuxR蛋白的背景浓度较低,如第3.1节所示。因此,发光强度的增加表明SM可能刺激了LuxR的表达。
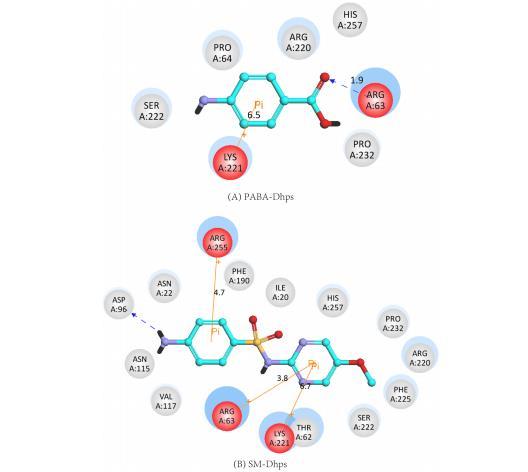
图4. PABA(A)与SM(B)与Dhps对接过程中的配体相互作用示意图。蓝色虚线与黄色实线分别表示配体与氨基酸残基之间的氢键及π-阳离子键。
从9到17小时,虽然浓度在1.07x10⁻⁵ 到 1.71x10⁻⁵ mol/L(LogC值在-4.97到-4.77之间)的SM刺激生物发光,但当SM浓度增加到1.92x10⁻⁵ 到 8.5x10⁻⁵ mol/L(LogC:在-4.72到-4.07之间)时,则产生抑制效应。此时期是细菌的指数期,细胞产生大量LuxR蛋白,这可能掩盖了SM对LuxR表达的刺激作用。分子对接可用于解释此期间高浓度SM的抑制效应。PABA和SM在Dhps结合位点的对接视图如图4所示,该图显示PABA通过两个氢键与Dhps蛋白的ARG-63和ARG-220残基结合,并通过pi-阳离子相互作用与LYS-221残基结合(图4A)。对于SM(图4B),虽然SM和Dhps的ASP-96之间只形成一个氢键,但SM和Dhps之间形成了三个pi-阳离子键,这表明Dhps-SM复合物比Dhps-PABA复合物更稳定。因此,SM可以与PABA竞争结合Dhps,从而停止对细菌生长至关重要的二氢叶酸的合成。因此,高浓度的SM抑制了费氏弧菌的发光。
相关新闻推荐
1、乳酸乳球菌的包埋体系LL@Fe-TA@mGN 生长曲线测定及胃肠道抗性与体内滞留能力(一)
2、淀粉芽孢杆菌、枯草芽孢杆菌抑制茄病镰刀菌效果显著,可促进黄瓜幼苗生长(一)
