
图2 、变形链球菌生物膜的表型特征。(A)用SYTO9和Alexa Fluor 647标记的葡聚糖偶联物标记24小时变形链球菌生物膜的细菌细胞和不溶性胞外多糖。绿色,细菌;红色,胞外多糖。图像在60×放大倍数下拍摄。使用Imaris 7.0.0进行细菌/胞外多糖生物膜的三维重建。(B)使用Imaris 7.0.0对细菌/胞外多糖生物量进行量化。结果是每个样本5个随机选择位置的平均值,并以平均值±SD表示
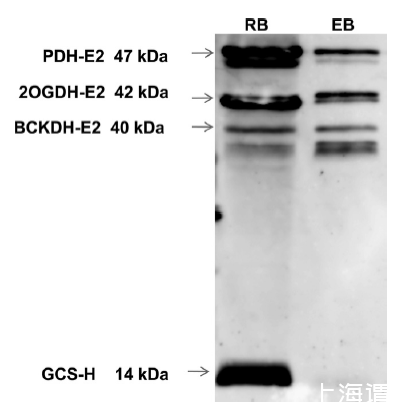
图3、 不同vicK突变菌株中VicRK调节子表达和变形链球菌胞外蛋白。(A)培养上清液的浓缩蛋白谱。从染色凝胶中提取培养上清液蛋白并进行质谱分析。M:标记;1:UASpec;2:VicKH217A;3:VicKP222A。(B)定量逆转录聚合酶链反应分析显示4种类型菌株的基因转录本。数值代表从3个不同实验获得的数据的平均值及标准差。使用Prism 7.0进行Student's t检验,P<0.001。误差线表示标准差。
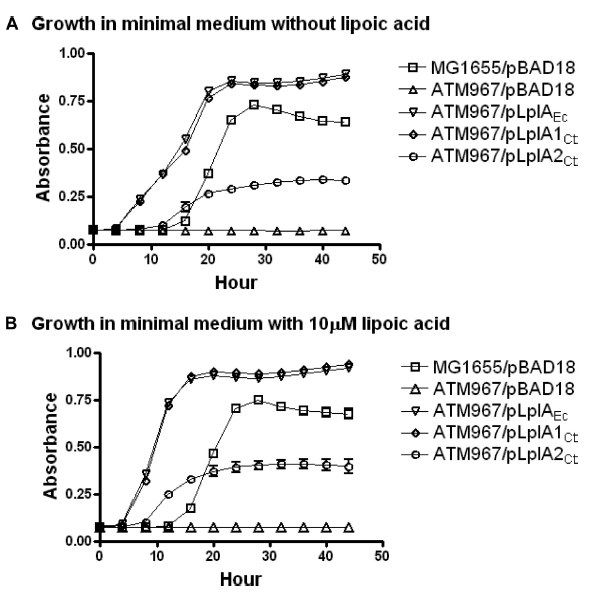
图4 、细胞中VicR-P的含量和VicRK调节子的转录分析。(A)含有在Todd-Hewitt酵母提取物培养液中指数生长的VicK突变菌株提取物的Phos-tag凝胶的代表性Western印迹。指示了未磷酸化VicR、VicR-P和一条非常微弱的污染条带的位置。虚线后的VicKP222A加热样品作为对照。(B)对照菌株UA、VicKP222A和两个vicR过表达突变体中参与生物膜形成的基因的表达谱。数据表示为平均值±SD。(C)含有在THYE培养液中指数生长的对照和突变菌株提取物的Phos-tag凝胶的代表性Western印迹。
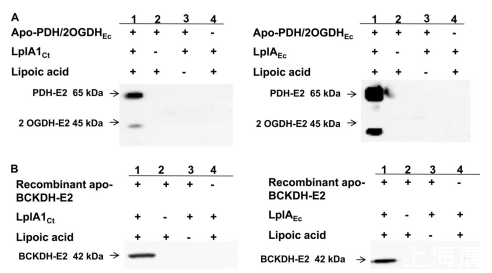
图5 、UASpec和VicKP222A的聚集。(A)UASpec和VicKP222A在新鲜未刺激全唾液存在下的聚集。点是重复三次的代表性实验的三次重复的平均值。使用Prism 7.0进行Student's t检验,*P< 0.05,**P<0.01,***P<0.005和****P<0.001。误差线表示标准差。(B)变形链球菌衍生菌株中spaP的转录分析。数据表示为平均值±SD,使用Prism 7.0进行Student's t检验,****P< 0.001。(C)突变菌株培养上清液中SpaP水平的代表性Western印迹分析。每个菌株的全细胞裂解液作为对照显示在Western印迹结果下方。M:标记;1:UASpec;2:VicKP222A;3:UASpec-His,在UASpec菌株中其SpaP蛋白结合His标签的突变体;4:VicKP222A-His,在VicKP222A菌株中其SpaP蛋白结合His标签的突变体。
总结
本论文的主要研究是关于变形链球菌中 VicK 双组分调控系统的磷酸酶功能如何影响细菌的聚集与生物膜形成。VicRK 是革兰阳性菌中高度保守的双组分调控系统,已知调控细胞分裂、细胞壁合成和生物膜形成,本研究人员首次 在 S. mutans 中通过定点突变分别阻断 VicK 的自磷酸化和磷酸酶活性,明确区分了两种功能的表型差异。发现 VicK^P222A 磷酸酶缺陷导致 VicR~P 积累高达 >90%(野生型仅约 9%),揭示了磷酸化水平的巨大变化,证明是 磷酸化的 VicR(而非总 VicR 量)决定了 gtfs 和 ftf 的表达调控。发现磷酸酶缺失导致 SpaP 黏附素下调,首次将 VicK 磷酸酶活性与 S. mutans 的唾液聚集能力联系起来,提出 VicK 磷酸酶活性可作为 新型抗菌靶点。
该研究首次明确了VicK的磷酸酶活性在变形链球菌中的核心调节作用。它通过精确调控VicR的磷酸化水平,进而影响细胞分裂、致龋性生物膜的关键基质合成以及细菌在唾液中的聚集行为。这些发现表明,靶向抑制VicK的磷酸酶活性,可能是一种调控变形链球菌生长、定植及其致病潜力的新颖策略。 Bioscreen 在本研究中发挥了定量评估突变株生长缺陷的关键作用。通过自动化、高频率的 OD600 监测,研究者精确地揭示了 VicK 磷酸酶缺失(VicK^P222A)导致 S. mutans 生长速度显著减慢的现象,为后续表型分析提供了基础数据支撑。该设备的高通量、连续监测能力使得不同菌株间的生长曲线对比更加准确和可靠。
Bioscreen 生长曲线分析仪被用于定量测定不同基因工程菌株在特定条件下的生长能力,是本论文中评估沙眼衣原体硫辛酸代谢相关基因功能的关键实验工具,Bioscreen 在本研究中扮演了 “生长表型量化器” 的角色。它通过自动化、多重复的监测,将“能否生长”这一生物学问题转化为精确、可比对的生长动力学数据,是连接基因构建(基因型)与功能验证(表型)之间的关键实验桥梁。
相关新闻推荐
1、生长曲线分析仪监测下吲哚对恶臭假单胞菌 ΔttgABC 突变体抗生素耐受的影响(四)
2、一株具有较强木质素降解能力的细菌XKG6生长最适宜PH与温度
