结果
原核表达载体pET28bTat-Sod-A/Tat-SodB/Tat-SodC与pET28b-Sod-A/SodB/SodC的构建
为阐明Tat蛋白标签对大肠杆菌异源蛋白表达的影响,本研究选取大肠杆菌Sod超家族基因(包括sodA、sodB和sodC),将其克隆至pET28b-Tat和pET28b载体中,构建了原核表达载体pET28b-Tat-Sod-A/Tat-SodB/Tat-SodC和pET28bSod-A/SodB/SodC。用于扩增这些基因的寡核苷酸序列如表1所示,原核表达载体构建示意图见图1。通过直接测序验证了原核表达载体的正确构建。
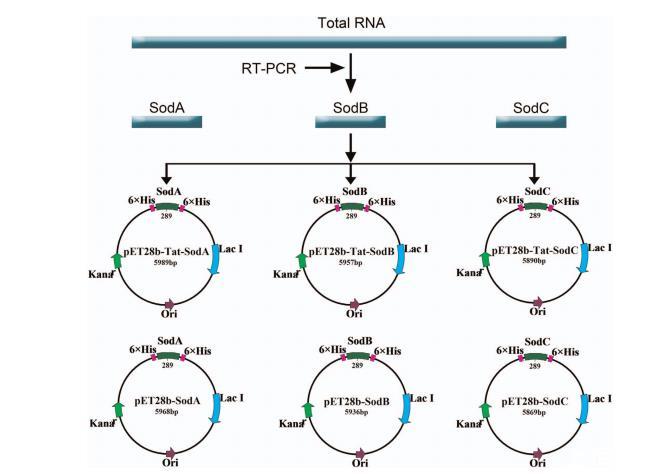
图1 原核表达载体构建示意图
Tat标签促进SodA、SodB和SodC在大肠杆菌中的高产量和可溶性表达
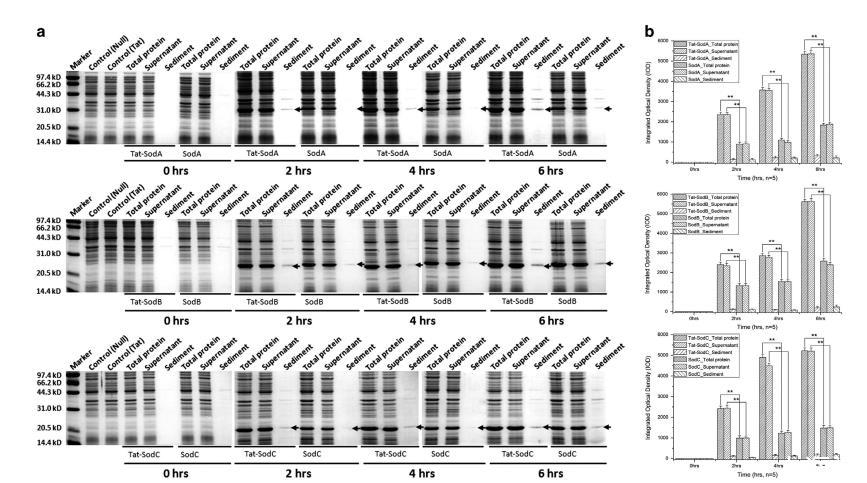
图2 通过SDS-聚丙烯酰胺凝胶电泳对Tat标签蛋白和无Tat标签蛋白进行蛋白表达水平测定。(a) 通过SDS-PAGE对Tat标签蛋白和无Tat标签蛋白进行蛋白表达水平测定。(b) Tat标签蛋白和无Tat标签蛋白表达水平的定量分析。星号表示菌株间具有统计学显著差异 (**P<0.01)。
为探究Tat标签对大肠杆菌异源蛋白表达的影响,分别在诱导后0、2、4和6小时收集细菌细胞,制备总蛋白(包括上清液和沉淀蛋白)。如SDS-PAGE电泳结果(图2a)及定量分析(图2b)所示,随着诱导时间的延长,Tat-SodC蛋白及不含Tat的蛋白(包括SodA、SodB和SodC)的表达量均呈现上升趋势。Tat标签蛋白的表达量显著高于不含Tat蛋白(2-5倍,**P<0.01),且两类蛋白主要定位于上清液,仅在沉淀组分中检测到微量表达。Western印迹分析(图3a)及定量结果(图3b)同样显示,Tat标签蛋白的表达水平显著高于不含Tat蛋白,且两类蛋白均主要存在于上清液,沉淀组分中仅检测到微量表达。
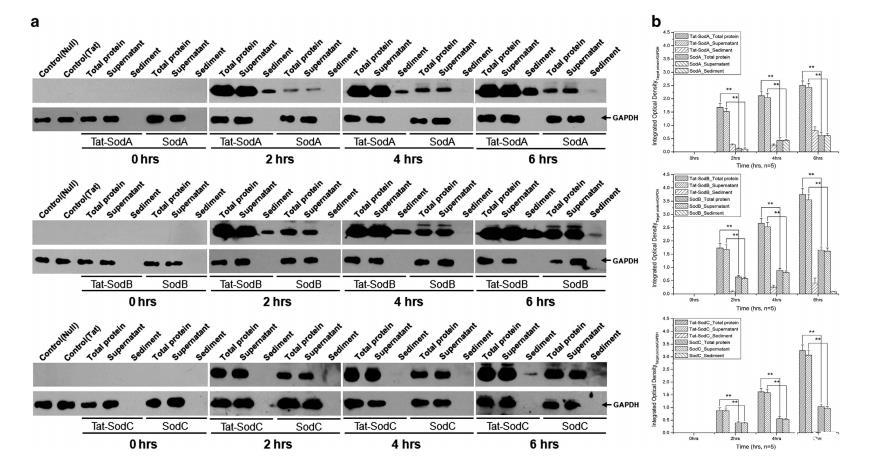
图3(a) 通过蛋白质印迹对Tat标签蛋白和无Tat标签蛋白进行蛋白表达水平测定。(b) Tat标签蛋白和无Tat标签蛋白表达水平的定量分析。星号表示菌株间具有统计学显著差异 (**P<0.01)。
Tat标签蛋白的总超氧化物歧化酶活性显著高于无Tat标签蛋白
为了阐明Tat标签蛋白和无Tat标签蛋白的总超氧化物歧化酶活性,在诱导后不同时间点收集细胞。随着诱导时间的增加,Tat标签蛋白和无Tat标签蛋白的总超氧化物歧化酶活性显著增加,并且Tat标签蛋白的活性显著高于无Tat标签蛋白,表现为SodA > SodC > SodB。
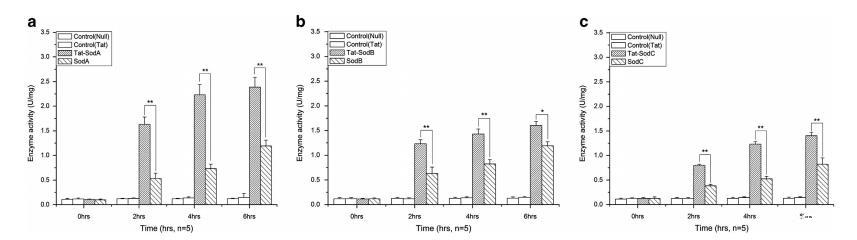
图4 Tat标签蛋白和无Tat标签蛋白的总超氧化物歧化酶活性测定。(a) Tat-SodA和SodA的总SOD活性测定。(b) Tat-SodB和SodB的总SOD活性测定。(c) Tat-SodC和SodC的总SOD活性测定。星号表示组间活性具有统计学显著差异 (*P<0.05; **P<0.01)。
表达Tat标签蛋白的细胞与表达无Tat标签蛋白的细胞相比,抗百草枯活性显著增加
为了研究Tat标签蛋白和无Tat标签蛋白的抗百草枯活性,在百草枯处理后,使用Bioscreen C测量了过表达Tat标签或无Tat标签SOD蛋白的大肠杆菌细胞在24小时内的生长曲线。经过4.0 mM百草枯处理后,与对照菌株相比,表达Tat标签蛋白和无Tat标签蛋白的细胞的生长随着诱导时间的增加而显著增加。此外,表达Tat标签蛋白的细胞的生长高于表达无Tat标签蛋白的细胞,表现为SodA > SodC > SodB。此外,与野生型相比,ΔSodA在培养6小时后的生长受到显著抑制,而ΔSodB和ΔSodC的生长受到轻微抑制。
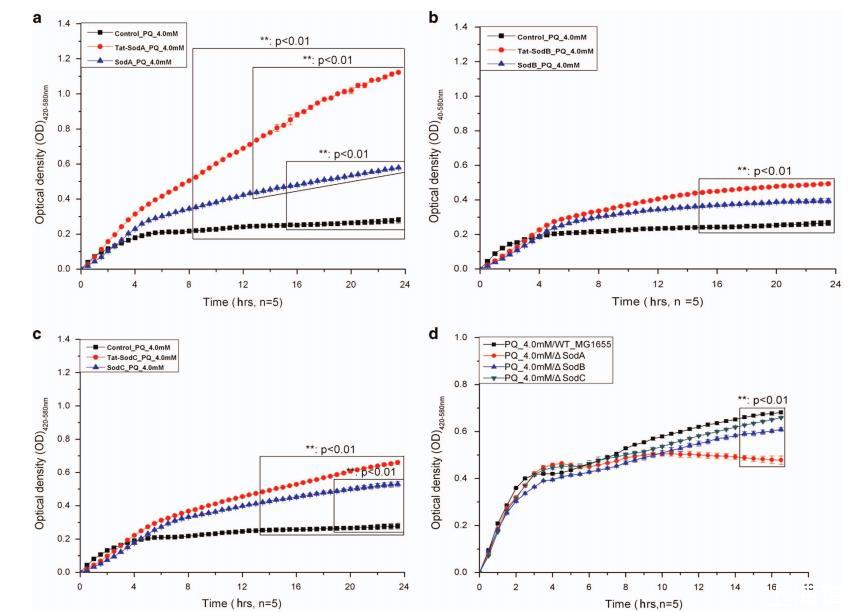
图5 过表达SodA、SodB和SodC的大肠杆菌菌株及ΔSOD突变菌株的细菌抗百草枯活性测定。(a) 过表达Tat-SodA和SodA菌株的细菌抗百草枯活性测定。(b) 过表达Tat-SodB和SodB菌株的细菌抗百草枯活性测定。(c) 过表达Tat-SodC和SodC菌株的细菌抗百草枯活性测定。
Tat标签的存在可能通过增加mRNA转录水平来促进异源蛋白在大肠杆菌中的高产量和可溶性表达
为了揭示Tat标签促进大肠杆菌中异源蛋白表达的机制,使用RT-qPCR检测了编码Tat标签蛋白和无Tat标签蛋白的基因的mRNA转录水平。在诱导蛋白表达后的0、3和6小时收集细胞并提取总RNA。如RT-qPCR测定结果所示,编码Tat标签蛋白和无Tat标签蛋白的sod基因的mRNA转录水平随着诱导时间的增加而显著增加,并且编码Tat标签蛋白的基因的mRNA转录水平比编码无Tat标签蛋白的基因高2-3倍。
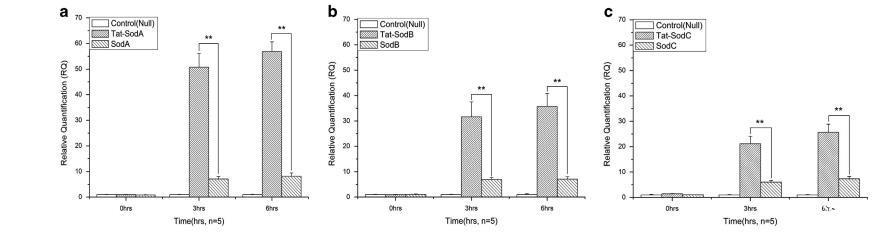
图 6 通过定量逆转录PCR对Tat标签蛋白和无Tat标签蛋白进行mRNA转录水平测定。(a) 通过RT-qPCR对Tat-SodA和SodA进行mRNA转录水平测定。(b) 通过RT-qPCR对Tat-SodB和SodB进行mRNA转录水平测定。(c) 通过RT-qPCR对Tat-SodC和SodC进行mRNA转录水平测定。星号表示蛋白质的转录水平间具有统计学显著差异 (*P<0.05; **P<0.01)。
