为了确认ClpP在体内调节HdiR的活性,我们通过Northern分析检测了野生型和clpP突变株的hdiR表达。结果表明,在缺乏ClpP的情况下,响应MMC和热的hdiR表达诱导比在野生型细胞中获得的诱导减少了四倍。因此,缺乏ClpP的细胞诱导HdiR调节子的能力受限,证明ClpP在体内调节其活性。
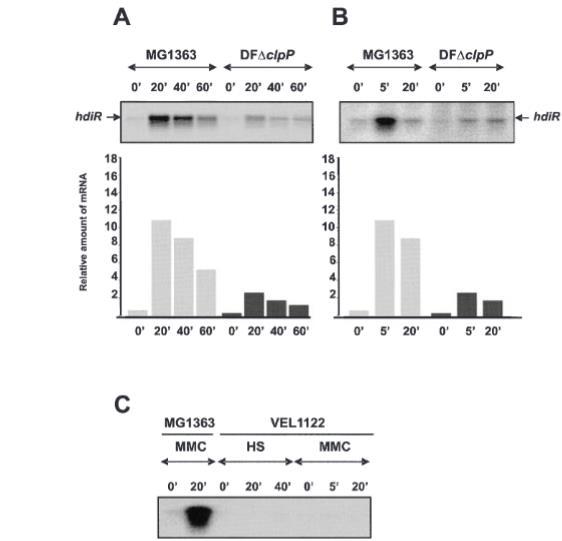
图7. 在MG1363、DFAclpP和VEL1122细胞中hdiR表达的Northern分析。A. 添加MMC前和添加后20、40、60分钟,MG1363和DFAclpP细胞中的hdiR表达。B. 热激前和热激后5、20分钟,MG1363和DFAclpP细胞中的hdiR表达。C. MMC处理的MG1363和VEL1122细胞以及热激处理的VEL1122细胞中的hdiR表达。柱状图显示相对mRNA诱导比率,通过将RNA样品的信号除以0分钟时MG1363细胞的信号计算得出。膜上的RNA量在rRNA杂交后进行校正。
HdiR是MG1363最佳生长所必需的
因为我们的数据表明HdiR的活性受热和MMC调节,我们希望确定HdiR在这些条件下是否对生存力很重要。因此,我们尝试构建一个缺失整个hdiR阅读框的缺失突变体。然而,我们多次尝试创建这样的菌株都未成功。或者,我们检测了野生型和PV114突变细胞在存在和不存在MMC的情况下以及在升高温度下的生长能力,发现两种菌株之间的菌落形成能力没有差异。然而,在所有测试条件下,PV114通常需要更长的培养时间才能形成与MG1363相同大小的菌落。PV114用一个编码HdiR但不编码下游YnaA的质粒进行回补,得到KS74。pKS47也被导入MG1363,得到KS73。使用Bioscreen监测系统测量了携带载体pCI372的KS73、KS74及其亲本菌株的生长速率。在30°C无MMC条件下使用五个平行样品进行的生长实验结果显示,虽然MG1363的倍增时间为59.1分钟,但在PV114中增加到78.2分钟。当菌株在升高温度下培养时,PV114无法启动生长,而KS74、KS73和MG1363则呈指数生长,倍增时间分别为149.8分钟、138.2分钟和152.8分钟。这些结果表明,当HdiR缺乏HTH结构域时,菌株存在生长缺陷,在所用条件下会消除其在高温下的生长。
讨论
在细菌细胞中,DNA损伤反应依赖于LexA样转录调节因子,这些因子在无DNA损伤时结合位于靶基因上游的DNA序列,并在DNA损伤时经历RecA介导的自切割以解除对靶基因表达的抑制。我们已经从革兰氏阳性菌乳酸乳球菌中表征了一种转录调节因子HdiR,它具有几个LexA样特征,包括其自身合成的负性自调控、被MMC诱导以及在保守的Ala和Gly残基之间的自切割。在LexA样自切割之前,RecA结合单链DNA区域,同时聚合成核蛋白丝。这种变化使RecA能够在LexA、UmuD和噬菌体阻遏蛋白的自切割反应中充当辅蛋白酶。因此,类似的RecA激活可能先于HdiR自切割。
当评估暴露于MMC的野生型细胞中过表达HdiR的稳定性时,只有两个HdiR切割产物中较大的N端部分可见,该片段的半衰期约为22分钟。然而,在缺乏编码Clp蛋白酶复合物蛋白水解亚基的clpP的情况下,两个切割产物都被稳定,表明它们是该蛋白酶的靶标。奇怪的是,我们还注意到clpP突变基本上消除了MMC对hdiR表达的诱导,表明携带HTH基序的N端HdiR切割产物保留了其DNA结合能力。这一观点得到了凝胶阻滞研究的证实,其中切割的HdiR阻滞了hdiR和umuC启动子片段。Clp蛋白水解复合物先前已被认为参与自切割产物的降解。UmuD'被ClpXP迅速降解以避免过量诱变,并且在最近的研究中,自切割LexA的产物也被证明是ClpXP蛋白酶的底物。因此,Clp蛋白水解复合物似乎在自切割蛋白质产物的周转中起着保守的作用。就HdiR而言,Clp蛋白水解复合物调节DNA损伤反应,因为N端切割产物仍然可以抑制基因表达,只有当被ClpP降解时,才对DNA损伤产生反应。LexA DNA结合结构域积累对DNA损伤后细胞生存的有害影响表明在大肠杆菌中存在类似的调控机制。
除了MMC,hdiR表达也被热诱导。虽然HdiR在这些条件下不稳定,但比存在MMC时稳定三倍。然而,在施加热激后约5分钟就达到了hdiR表达约15倍的诱导,而当细胞用MMC胁迫时需要20分钟才能达到相同水平,表明HdiR的稳定性在热应激下去抑制HdiR调节子中不起关键作用。然而,hdiR表达的热诱导在recA突变细胞中完全被消除,并且在缺乏clpP的情况下大大降低,证明RecA和ClpP对热激诱导都显然很重要。虽然可能涉及其他蛋白质,但我们的数据表明,HdiR调节子的DNA损伤诱导和热介导诱导涉及共同的元件。
LexA同源物存在于许多细菌中,特别是在那些具有较大基因组的细菌中。奇怪的是,葡萄球菌同时含有HdiR和LexA同源物,表明这两种蛋白质具有独立的生物学功能。然而,乳酸球菌和链球菌物种似乎缺乏LexA,因此HdiR可能是这些生物中DNA损伤反应的调节因子。为了解决这个问题,我们多次尝试鉴定HdiR靶基因;然而,我们只在乳酸乳球菌MG1363中鉴定了hdiR,而umuC是乳酸乳球菌IL1403中HdiR的靶标。此外,我们专门检测了recA表达是否被HdiR抑制,但未检测到表达HdiR'的野生型和PV114突变细胞之间的任何差异。根据最近的一项研究,其中显示球形红细菌的LexA既作为基因表达的阻遏物又作为激活剂发挥作用,我们也检测了HdiR是否是recA表达的正调节因子。在将野生型和hdiR突变细胞暴露于MMC后,我们发现recA仅被轻微诱导,并且这种诱导在携带缺乏HTH结构域的HdiR'的细胞中略有降低。因此,HdiR对recA表达仅有边际影响。
当我们检测表达HdiR'的突变细胞的表型时,我们发现它们对MMC的抵抗性与野生型细胞一样,但无法在高温下生长。因此,由HdiR控制的基因的适时表达似乎是高温生长所必需的。然而,为了理解结果的生理意义,我们需要更多关于HdiR调节子的信息。在本文中,我们已经表明HdiR的N端半部分在自切割后保持活性。有趣的是,发现蛋白质的C端半部分高度不稳定,并且仅在缺乏ClpP的细胞中检测到,表明它也可能具有重要的生物学功能。
在我们的研究中,我们鉴定出一种新型转录调节因子,其表达响应DNA损伤和热应激。乳酸乳球菌中热激和DNA损伤反应之间的联系先前已被以下发现所暗示:破坏乳酸乳球菌recA基因导致温度敏感性,并且这种敏感性被破坏一个基因trmA所抑制,该基因也抑制clpP突变的温度敏感性。我们目前的发现表明HdiR可能是这样的一个联系。
相关新闻推荐
1、疫苗候选菌株:猪胸膜肺炎放线杆菌生长曲线、溶血活性、 耐药性测定(一)
