接下来,我们检测了RecA是否在体内刺激HdiR自切割。然而,染色体表达的HdiR在存在或不存在热或MMC的情况下都无法通过蛋白质印迹分析检测到。因此,我们通过从携带插入组成型启动子后面的hdiR基因的质粒过表达HdiR来促进检测。将所得质粒pKS49转移到野生型和recA突变株VEL1122中,分别得到菌株KS78和KS80。随后,我们通过将两种菌株暴露于MMC,然后用氯霉素抑制蛋白质合成,检测了HdiR在DNA损伤条件下的稳定性。在所示时间点,通过蛋白质印迹分析蛋白质提取物。结果显示,在缺乏RecA的菌株中,添加CAM后45分钟,HdiR的量保持不变,而在RecA存在的情况下,HdiR被迅速切割,在阻断蛋白质合成30分钟后基本上没有未处理的HdiR。这些结果表明,HdiR在体内的自切割依赖于RecA。
因为hdiR被热诱导,我们接下来研究了RecA介导的HdiR自切割是否也发生在热应激条件下。当如上所述分析HdiR的体内稳定性时,我们发现野生型细胞中完整HdiR的量在添加CAM后虽然缓慢,但确实减少了,而HdiR在recA突变细胞中保持稳定。此外,我们在recA突变细胞中未能检测到切割产物,而从野生型细胞获得的样品中出现少量约14 kDa的片段,表明HdiR的自切割也发生在热激条件下。然而,由于在热应激期间似乎只发生低水平的自切割,我们希望确定recA在这些条件下是否在诱导hdiR表达中起作用。当我们检测recA突变细胞中的hdiR表达时,我们发现,正如预期的那样,在没有RecA的情况下,MMC的诱导被消除。我们还观察到,在缺乏RecA的细胞中,热的诱导完全被消除,证明RecA确实是hdiR热诱导所必需的。
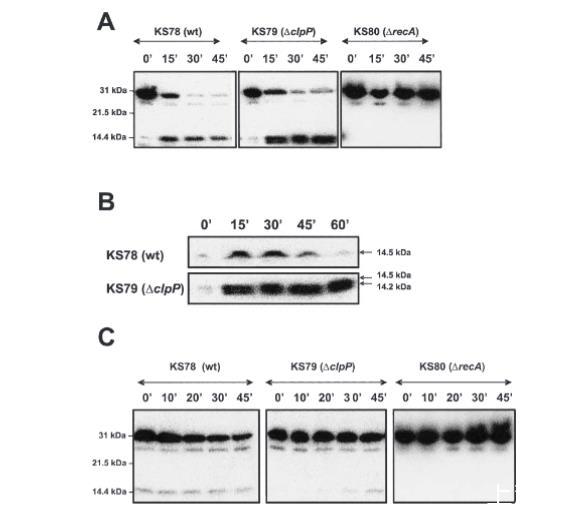
图5. HdiR的体内稳定性。A. 用MMC处理的KS78、KS79和KS80细胞,在添加CAM后0、15、30和45分钟取样。B. 用MMC处理的KS78和KS79细胞,在添加CAM后0、15、30、45和60分钟取样。C. 从25°C转移到38.5°C的KS78、KS79和KS80细胞,在添加CAM后0、10、20、30和45分钟取样。蛋白质样品通过SDS-PAGE分析,然后用抗His6-HdiR抗体进行Western印迹。在所有蛋白质样品中,一个未知的、与HdiR过产无关的蛋白质,迁移在未处理的HdiR下方,被抗体识别。该蛋白质用作上样等量蛋白质样品的内参。
ClpP调节HdiR活性
根据几项独立的Northern分析,hdiR表达的最大诱导水平在添加MMC后15到30分钟之间达到。当比较响应MMC的hdiR表达相对缓慢的诱导与相同条件下过表达HdiR的快速自切割时,结果表明HdiR的切割可能不足以诱导表达。因此,我们检测了自切割HdiR的DNA结合活性。有趣的是,在pH 10下孵育过夜的HdiR在凝胶迁移实验中仍然能够阻滞hdiR和umuC启动子片段,其中DNA-蛋白质复合物的迁移比含有等量HdiR在pH 7下孵育的反应更快。这些结果表明HdiR切割产物仍然能够结合靶序列。
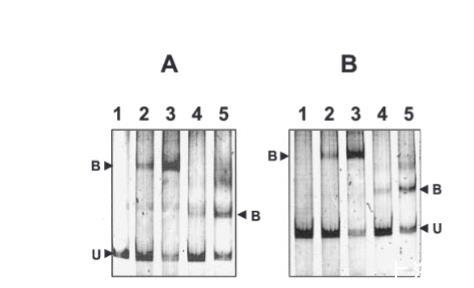
图6. 自切割HdiR的DNA结合能力。A. 含有hdiR启动子片段和分别在pH 7.0和pH 10孵育的His6-HdiR的反应。B. 含有umuC启动子片段和分别在pH 7.0和pH 10孵育的His6-HdiR的反应。第1道指不含His6-HdiR孵育的启动子片段。未结合DNA和蛋白质-DNA复合物的位置如图所示。
当观察HdiR的体内自切割时,我们注意到只有14.5 kDa的N端切割产物可见,并且这个产物似乎也不稳定。鉴于HdiR与LexA和UmuD相似,两者在处理后都是Clp蛋白水解复合物的靶标,我们检测了HdiR在缺乏ClpP的菌株中的稳定性。添加MMC后,我们发现未处理HdiR的半衰期在缺乏ClpP的情况下与野生型细胞相比增加了约30%。此外,在clpP突变体中,两个HdiR切割产物都可见,并且在野生型细胞中14.5 kDa片段的半衰期为22分钟±2分钟,而该片段在clpP突变细胞中没有被降解。这些结果表明两个HdiR切割产物都是Clp蛋白酶的靶标。
接下来,我们研究了ClpP对热激后HdiR稳定性的影响,发现虽然HdiR的量在野生型细胞中减少,但在缺乏ClpP的细胞中没有检测到显著变化。此外,在野生型细胞的所有时间点都可以检测到14 kDa的微弱条带,而在clpP突变株中,只有在添加CAM后45分钟取样的样品中才能检测到。
