2.2副干酪乳杆菌Lab5菌液与热灭活菌液的抗菌活性
为确定不同组分发酵菌液的抑菌活性,制备灭活发酵上清液、灭活菌悬液、细胞裂解物进行抑菌实验,结果如图2、表3所示,发现只有灭活CFS对指示菌有抑菌效果,说明具有抑菌效果的物质存在于发酵上清液中。Behrooz等也发现副干酪乳杆菌B31-2的发酵上清液对单增李斯特菌表现出显著抗菌活性,这与本文结果一致,但并未进一步阐明其他组分是否具有抑菌效果。
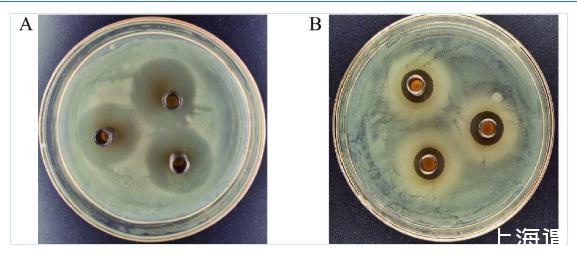
图 2 副干酪乳杆菌Lab5发酵上清液对不同指示菌的抑菌活性
注:A为指示菌ListeriamonocytogenesATCC19115;B为指示菌EscherichiacoliATCC25922。
表 3 副干酪乳杆菌Lab5发酵菌液不同组分对指示菌生长性能的影响
| 指标 | 10~8分 | 6~8分 | 4~6分 | 2~4分 | 0~2分 |
|---|---|---|---|---|---|
| 色泽 | 鲜亮有光泽 | 较鲜亮有光泽 | 暗红无光泽 | 暗灰无光泽 | 暗褐无光泽 |
| 气味 | 鲜味强无异味 | 鲜味较强无异味 | 鲜味淡略有异味 | 无鲜味儿异味较大 | 无鲜味,重异味且不能接受 |
| 弹性 | 弹性很好,指压后立即恢复 | 弹性较好,指压后可以恢复 | 弹性较差,指压后缓慢恢复 | 弹性基本丧失,指压后不能恢复 | 无弹性,指压后凹陷明显不恢复 |
| 粘度 | 外部微湿不黏手 | 外部湿润不黏手 | 外部干燥微黏手 | 外部干燥较黏手 | 外表有粘液很黏手 |
| 大理石纹理 | 纹理清晰,花纹丰富 | 纹理清晰,花纹丰富 | 纹理不清晰,花纹微丰富 | 纹理模糊,有少量花纹 | 无纹理 |
注:“−”表示抑菌圈≤8mm,即无抑菌圈、无抑菌活性。
2.3副干酪乳杆菌Lab5发酵上清液抑菌活性的热稳定性
热稳定性实验结果如图3,发现随温度的升高,发酵液抑菌活性降低。但经60、70、80、90、100、121℃处理后,副干酪乳杆菌Lab5CFS对单增李斯特菌仍保持较高抑菌活性且无显著性差异(P>0.05)。经100、121℃处理后发酵上清液与对照组相比,对大肠杆菌的抑菌活性有差异但不显著(P>0.05)。121℃处理25min后,副干酪乳杆菌Lab5CFS对单增李斯特菌和大肠杆菌抑菌圈仍分别达到32.07±2.1mm、11.53±0.44mm,以上结果表明副干酪乳杆菌Lab5CFS热稳定性好。
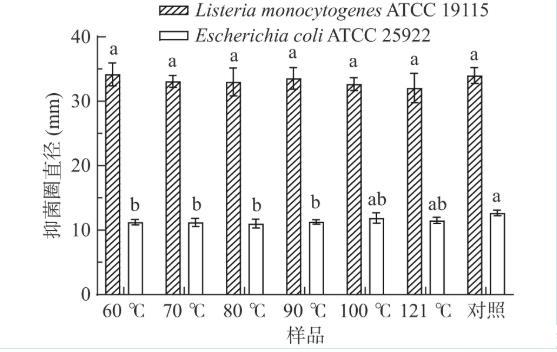
图 3 温度对副干酪乳杆菌Lab5发酵上清液抑菌活性的影响
注:图中不同小写字母代表不同温度处理组对指示菌(ListeriamonocytogenesATCC19115或EscherichiacoliATCC25922)抑菌圈直径的差异显著(P<0.05),图4~图5同。
Huang等发现乳酸菌发酵液粗提物的抗菌活性在40~100℃间具有较高的稳定性,而在121℃下抑菌面积减少约26.15%。副干酪乳杆菌Lab5CFS经121℃处理后对单增李斯特菌的抑菌面积减少10.87%。良好的热稳定性对其应用于食品加工是非常有利的。
2.4副干酪乳杆菌Lab5发酵上清液抑菌活性的蛋白酶敏感性
选取6种代表性蛋白酶进行抑菌实验,探究其蛋白酶敏感性(图4),与对照组相比,热灭活副干酪乳杆菌Lab5CFS经蛋白酶处理后抑菌活性均下降,蛋白酶K组对单增李斯特菌和大肠杆菌的抑菌活性影响最大(P<0.05),抑菌圈直径分别为26.33±0.74mm、8.84±0.56mm,比对照组减小了7.69mm、3.18mm;胃蛋白酶组对单增李斯特菌和大肠杆菌抑菌圈直径分别减小5.39mm、2.87mm。经蛋白酶处理后抑菌活性下降,热灭活副干酪乳杆菌Lab5CFS中可能含有蛋白质或肽类抑菌物质。不同于许多乳酸菌株CFS对蛋白酶表现出高敏感性特征,经蛋白酶K、胃蛋白酶、胰蛋白酶和木瓜蛋白酶处理后完全丧失活性。副干酪乳杆菌Lab5CFS经蛋白酶处理后虽抑菌活性下降但仍有较好抑菌效果,结果表明其对六种蛋白酶较不敏感,在食品工业中具有很好的应用潜力。
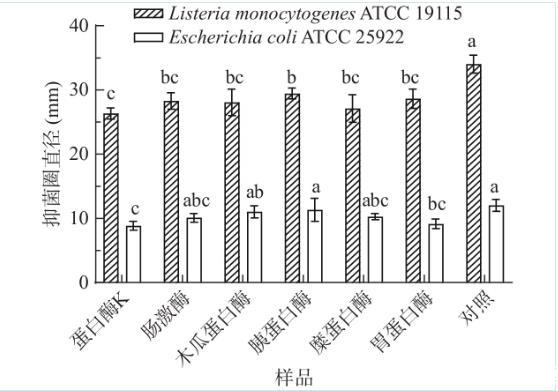
图 4 蛋白酶处理对热灭活副干酪乳杆菌Lab5发酵上清液的抑菌活性的影响
2.5副干酪乳杆菌Lab5发酵上清液抑菌活性的pH稳定性
如图5所示,将灭活副干酪乳杆菌发酵液的pH调整至不同pH处理1h,在pH3.0~8.0时抑菌活性未发生显著变化(P>0.05),在接近初始pH3.51的pH4时抑菌活性降低最少,当pH9.0时,副干酪乳杆菌Lab5灭活发酵上清液抑菌活性显著降低(P<0.05)。在强碱性条件下,副干酪乳杆菌LabCFS抑菌活性降低可能是由于其中含有乳酸、乙酸等有机酸,有机酸因解离而失去抑菌活性。乳酸菌代谢产物具有广谱抑菌性,其抑菌活性具有酸依赖性,例如乳酸链球菌代谢产物,而副干酪乳杆菌Lab5灭活发酵上清液在pH3.0~8.0范围内pH稳定性好,为其在猪肉等食品保鲜中应用提供了可能性。
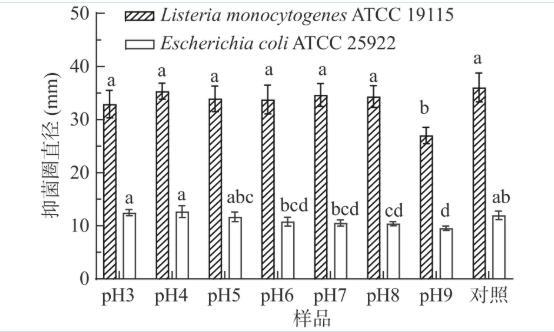
图 5 pH对热灭活副干酪乳杆菌Lab5发酵上清液的抑菌活性的影响
2.6副干酪乳杆菌Lab5生长曲线及其灭活CFS抑制单增李斯特菌的最小抑菌浓度
生长曲线如图6,OD600nm值显示培养6~18h即进入对数生长期,20h左右进入稳定期。pH在培养6h后开始发生变化,6~24hpH迅速下降,从5.33降至3.86,24~41hpH缓慢下降,41h后恒定在3.5左右。抑菌实验结果显示副干酪乳杆菌生长开始产生抑菌物质,培养44h时抑菌活性达到最高,随后保持稳定。整个过程与pH的变化无关,结果表明副干酪乳杆菌Lab5在整个生长期间一直产生抑菌物质。
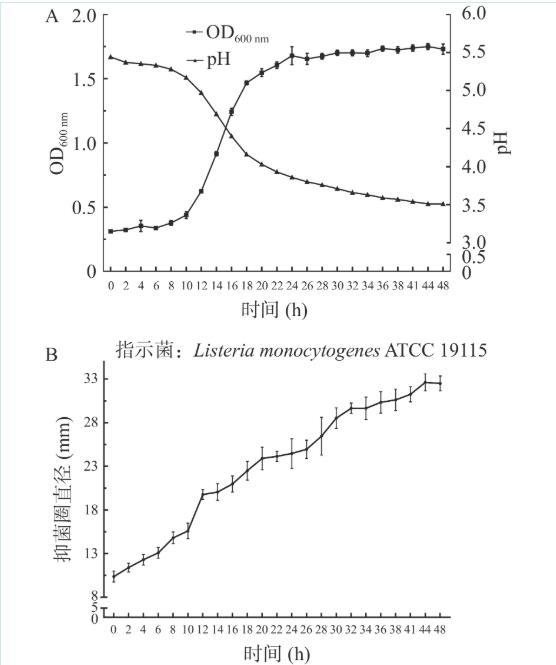
图 6 副干酪乳杆菌Lab5的生长曲线及抑菌活性
微量肉汤稀释法结果显示灭活副干酪乳杆菌Lab5CFS低于12.5mg/mL时单增李斯特菌可以生长,而12.5mg/mL浓度处理下的OD600nm值与阴性对照组无显著差异,表明ListeriamonocytogenesATCC19115生长完全受到抑制,因此确定其对单增李斯特菌的MIC为12.5mg/mL。
