两个BirA同源物的表征
在益生菌乳酸球菌中,利用冗余基因破译一种独特的生物素,BPL被分为两组:I组BPL缺乏N端DNA结合基序,而II组BPL(BirAs)具有N端DNA结合域。范式II组BPL是大肠杆菌BirA,此类酶也存在于古菌中,表明II组版本可能是BPL酶家族的祖先。基于注释,乳酸乳球菌IL1403可能拥有两种类型的BPL,此处称为BirA1_LL(323个残基,推定的II组BPL)和BirA2_LL(250个氨基酸,推定的I组BPL)。两个BirA蛋白的多序列比对显示,它们与大肠杆菌BirA相比,具有20.7%的同一性和34.6%的相似性(图2)。
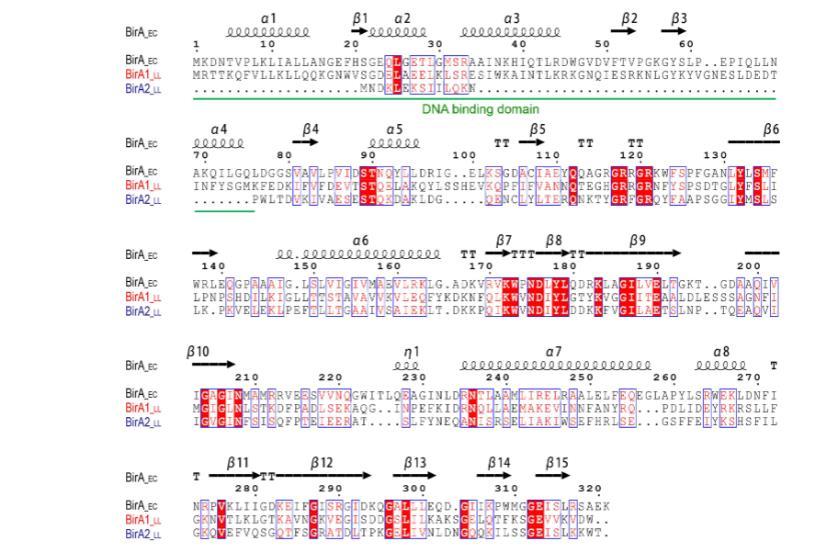
图2.乳酸乳球菌BirA同源蛋白与大肠杆菌BirA的序列比对。多序列比对使用ClustalW2,软件完成,最终输出结果经ESPript 2.2.程序处理。本研究采用大肠杆菌K-12 MG1655(登录号AAC43075)的BirA_ec蛋白作为参照,乳酸乳球菌IL1403的两个BirA同源蛋白作为参考序列。其中,红色标注的为BirA1_LL(登录号NP_267937),蓝色标注的为BirA2_LL(登录号NP_268060)。相同残基以白色字母配红色背景显示,相似残基以红色字母配白色背景显示,不同残基以黑色字母显示,空位用圆点表示。比对顶部展示了BirA的预测二级结构:其中,“α”代表螺旋结构,“β”代表片层结构,“T”代表转角/卷曲结构。标注说明:EC为大肠杆菌,LL为乳酸乳球菌。
为了测试两个乳酸乳球菌IL1403 BirA蛋白的BPL活性,我们纯化了六组氨酸标签蛋白至均质。纯化重组蛋白的SDS-PAGE图谱表明BirA1约为40 kDa,而BirA2_LL估计约为30 kDa(图3A)。为了进一步验证其身份,使用MALDI-TOF分析消化的多肽片段。MS结果支持两个纯化的重组蛋白是BirA1_LL(覆盖率36.8%)和BirA2_LL(覆盖率45.6%)(图3B,C)。
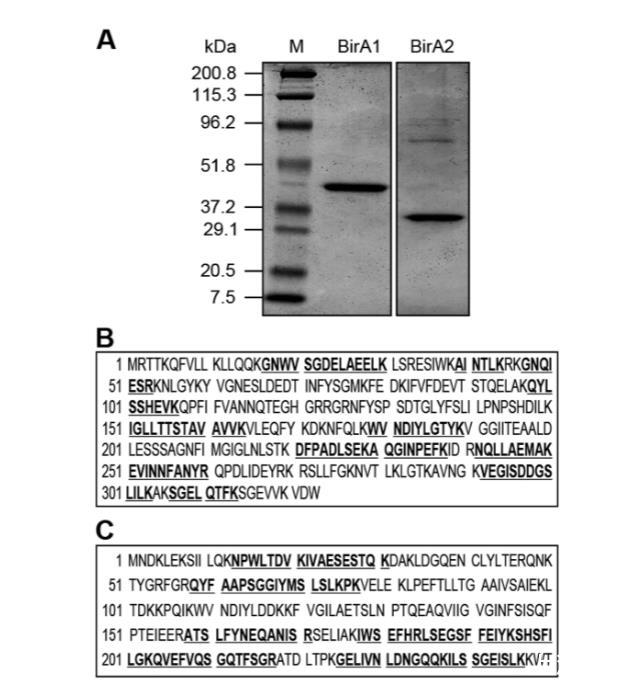
图3.乳酸乳球菌BirA1和BirA2蛋白的纯化及质谱鉴定。(A)两种纯化BirA蛋白(BirA1和BirA2)的12%SDS-PAGE电泳图谱。首条泳道使用预染色蛋白标准品(M),图左侧标注了各分子量单位(kDa)。通过液相色谱四极杆飞行时间质谱验证两种重组蛋白BirA1(图B)和BirA2(图C)的鉴定结果。与数据库序列匹配的肽段片段以加粗下划线形式标注。BirA1的覆盖率为36.8%,BirA2的覆盖率为45.6%。
为了更好地可视化乳酸乳球菌两种不同形式BPL的结构,进行了结构建模。与大肠杆菌BirA相似(图4A),BirA1_LL也具有N端DNA结合基序和C端酶结构域(图4B,C),符合II组BPL的标准。BirA2_LL的结构与嗜热氢菌BirA(I组BPL成员)几乎相同(图4D-F),支持其分类为I组BPL。
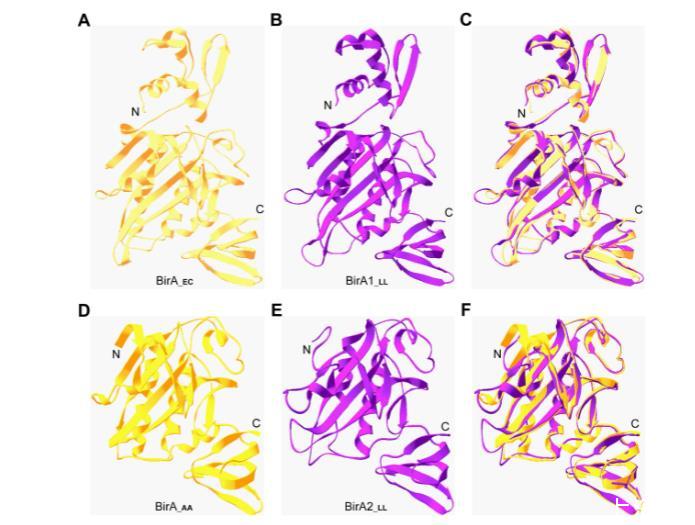
图4.乳酸乳杆菌两种BirA同源蛋白的结构解析。大肠杆菌BirA结构(图A)与乳酸乳杆菌BirA1(BirA1_LL)的建模结构(图B)具有高度结构相似性。(C)BirA1_LL与BirA_EC的结构叠加对比。BirA_EC结构(PDB:1HXD)以黄色标注,而与BirA_EC结构同源性达28.6%的BirA1_LL结构则以紫色呈现。(D)嗜热栖热菌BirA蛋白(BirA_AA)的整体结构视图,以及以BirA_AA为模板建模的BirA2_LL蛋白(图E/F)结构叠加对比。BirA_AA结构(PDB:3EFS)以金色标示,而以BirA_AA为模板、同源性达32.4%的BirA2_LL建模结构则以紫色高亮显示。标注说明:AA代表嗜热栖热菌;LL代表乳酸乳杆菌;N表示N端;C表示C端。
比较两个乳酸乳球菌BirA蛋白的BPL活性
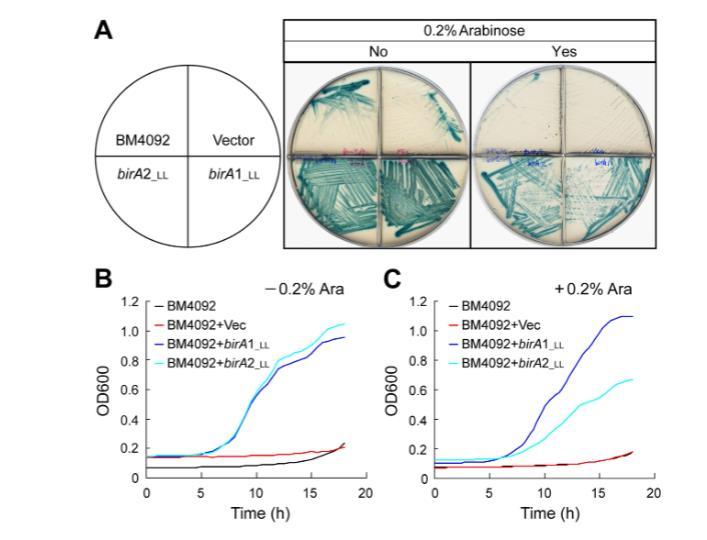
BPL活性使用充分研究的大肠杆菌模型和体外酶测定进行测量。用于功能互补birA同源物的模型大肠杆菌菌株是birA1突变体BM4092,它缺乏合成生物素或高亲和力转运生物素的能力2?。正如预期,BM4092菌株无论带有或不带空载体pBAD24,在补充25 nM生物素的M9琼脂平板上均不生长(图5A)。相反,阿拉伯糖诱导表达(甚至基础表达)的birA1_LL和birA2_LL均支持BM4092在非允许生物素水平(25 nM)下生长(图5A)。
BM4092衍生物在液体培养基中的细菌生长曲线也给出了与琼脂平板相似的结果(图5B,C)。值得注意的是,birA1_LL的过表达似乎对大肠杆菌有轻微毒性,因为添加0.2%阿拉伯糖的BM4092菌株生长与缺乏诱导剂阿拉伯糖的条件相比显著抑制(图5C)。总之,这些数据提供了体内证据,表明乳酸乳球菌的两个BirA直系同源物(BirA1_LL和BirA2_LL)具有BPL活性。
随后,使用体外测定进一步比较了BirA直系同源物的BPL功能,以评估生物素化活性。在此反应中,包括了三个版本的BirA(BirA_ec、BirA1_LL和BirA2_LL),并使用BPLs靶向的AccB蛋白结构域(指定为AccB87或BCCP87)作为底物(图6A)。原则上,AccB87第122位保守赖氨酸(K122)应在功能性BPL存在下被生物素化(图1A)。使用薄层色谱(TLC)直接可视化BPLs将α-32P标记的ATP和生物素转化为中间产物生物素酰-AMP(图1A)(图6B)。

TLC方法还提供了第二个连接酶部分反应的间接证据,该反应在引入受体蛋白AccB87时发生(即,将生物素从生物素酰-5'-AMP转移到AccB87赖氨酸),导致生物素酰-5'-AMP中间体损失和AMP形成(图1A和6B)。在AccB87存在下ATP消耗增加(尤其是BirA-ec)是由于在缺乏受体蛋白时,生物素酰-AMP仍紧密结合在连接酶活性位点内,因此每个连接酶分子仅形成一个生物素酰-AMP分子(即生物素酰-AMP合成不是催化性的)。生物素转移到受体蛋白允许催化和持续将ATP转化为生物素酰-AMP。这些结果进一步证实了BPL活性。
我们的结果表明,乳酸乳球菌的两种BirA蛋白都具有将生物素和[α-32P]-ATP转化为典型生物素酰-5'-AMP中间体的能力(图6B),并间接支持将生物素部分转移到AccB87受体蛋白(图6B)。BirA1_LL和BirA2_LL之间最显著的区别是,在添加受体蛋白后,BirA2_LL测定中AMP与ATP的比率明显高于BirA1_LL测定,并且BirA2_LL似乎形成更多的生物素酰-5'-AMP中间体(图6B)。这表明BirA2_LL催化生物素附着的速度比BirA1_LL快。大肠杆菌BirA消耗了大部分α-32P标记的ATP,而在乳酸乳球菌BirA测定中未观察到ATP消耗的明显增加(图6B)。
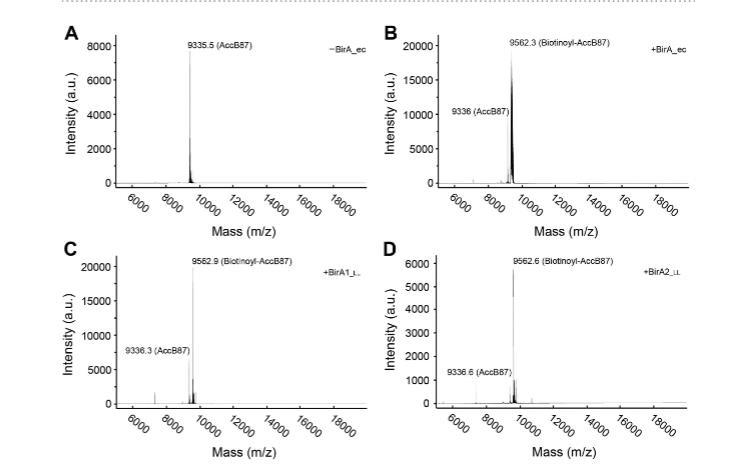
这意味着在测试条件下,BirA_ec是三个BPL酶中最活跃的版本。使用MALDI-TOF直接测量由生物素化引起的AccB87质量变化,如先前所述。在我们的测定中,AccB87的质量计算为9335.5~9336.6(图7A),生物素酰-AccB87的质量确定为9562.3~9562.9(图7B-D)。总之,数据说明:1)乳酸乳球菌两种版本的BirA(BirA1_LL和BirA2_LL)作为BPLs功能较弱;2)BirA2_LL相对于BirA1_LL更具催化活性。
相关新闻推荐
1、新型靶向抗癌药HDAC抑制剂可诱导肿瘤细胞分化、选择性凋亡——结果与讨论
3、不同盐度下纤毛虫(黄色伪角毛虫和扇形游仆虫)的生长曲线(一)
