残留角蛋白在通过Whatman 2号滤纸去除底物并在105°C下干燥后测定。
粗培养液中蛋白酶和角蛋白酶的特性
蛋白酶和角蛋白酶的最适温度在30-60°C范围内,以5°C为间隔,在0.1 M Tris-HCl缓冲液,pH 7.4中测定。pH的影响在pH 5-11范围内测试,使用0.1 M Britton-Robinson通用缓冲液,在最适温度下进行。为了确定粗培养液中蛋白酶和角蛋白酶的主要催化类型,在酪蛋白或可溶性角蛋白上的反应在最适条件下进行,之前用以下抑制剂进行20分钟预处理:PMSF(苯甲基磺酰氟)、NEM(N-乙基马来酰亚胺)、EDTA(乙二胺四乙酸二钠盐)和激活剂:半胱氨酸、CaCl₂。
酶谱法
在酶谱分析之前,使用Labscale TFF系统(Millipore)和带有Ultracel-10 PLCGC膜(10 kDa截留分子量)的Pellicon XL 50盒浓缩培养液。浓缩的培养上清液与样品缓冲液(Tris-HCl 0.32 M;pH 6.8;甘油48%;SDS 8%;溴酚蓝0.06%)以6:4的比例混合。将样品上样到含有酪蛋白/明胶0.1%的8%聚丙烯酰胺凝胶(5%积层胶)上。电泳在2°C下以20 mA进行5.5小时。电泳后,凝胶用Triton-X 2.5%洗涤两次,用孵育缓冲液(Tris-HCl缓冲液0.05 M,pH 8.6,含CaCl₂5 mM和叠氮化钠0.02%)洗涤一次,并在相同缓冲液中于30°C孵育24小时。为了条带检测,凝胶用考马斯亮蓝染色,并用甲醇:乙酸:水(50:10:40)脱色。
结果
细菌鉴定和分子系统发育研究
先前研究中指定为B1pz的分离株在分子基础上被重新鉴定。将16S rDNA部分序列与RDP进行初步比较,揭示了与微球菌属成员的密切关系。
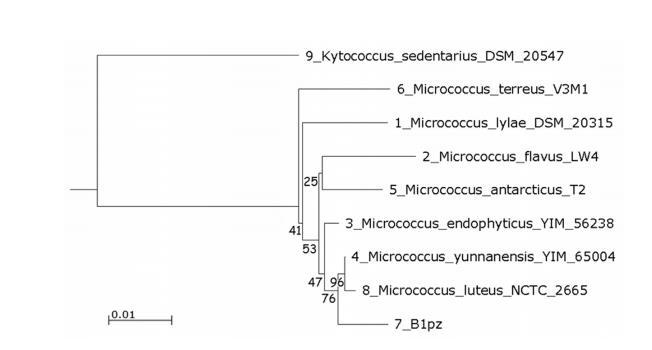
通过提交至GenBank数据库证实了与藤黄微球菌菌株NCTC 2665的高度相似性(100%)。在邻接系统发育树中,菌株B1pz与藤黄微球菌NCTC 2665和云南微球菌(M.yunnanensis)YIM 65004的一个亚分支密切相关,具有较高的自举值(图1)。该分离株被鉴定为藤黄微球菌(Micrococcus luteus),一种革兰氏阳性、需氧、不形成孢子的球菌,排列成细胞四联体并产生黄色色素。
羽毛肉汤培养基中的角蛋白酶生产
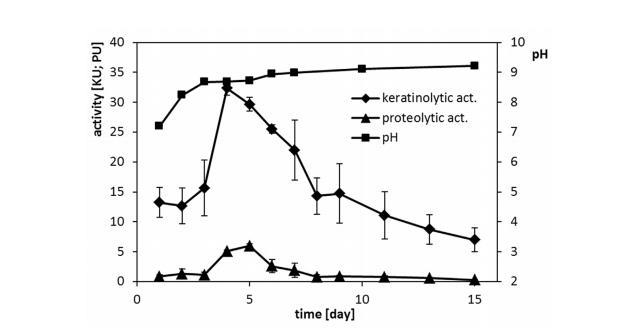
在15天的培养期间,藤黄微球菌B1pz菌株利用羽毛底物作为培养基中的主要营养源,同时伴随着细胞外蛋白酶的产生。角蛋白分解和酪蛋白分解活性的生产高峰出现在培养的第四天和第五天之间,最大值分别为32.3 KU和6.0 PU(图2)。培养基中的羽毛含量对目标酶的生物合成产生影响,影响底物利用率。在底物浓度为1-2%时,角蛋白分解活性水平相当,高于此水平时观察到生物合成显著下降(表1)。
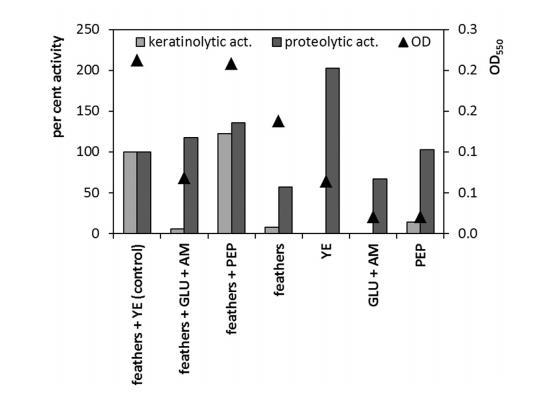
尽管如此,在2%羽毛含量时,酪蛋白分解蛋白酶的生产出现轻微刺激。向羽毛培养基中添加额外的补充剂也是角蛋白酶生产的关键因素。与含有羽毛和酵母提取物的对照培养基相比,添加蛋白胨导致最大角蛋白分解活性刺激了22%(图3)。葡萄糖几乎完全抑制了角蛋白酶的生产,但不影响蛋白水解活性。羽毛诱导物的存在对角蛋白酶的生物合成至关重要,但对酪蛋白分解蛋白酶则不然。然而,测试菌株在羽毛培养基中没有任何补充剂的情况下无法产生显著的角蛋白酶水平。
| 羽毛含量[%] | 角蛋白分解活性[KU] | 蛋白水解活性[PU] | pH | 蛋白质[mg/mL] | 氨基酸[mM] |
| 1 | 32.3±1.2 | 6.0±0.3 | 9.25 | 1.24 | 1.70 |
| 2 | 34.0±7.2 | 19.3±2.1 | 9.08 | 1.47 | 1.68 |
| 4 | 20.4±6.6 | 7.1±3.2 | 9.05 | 0.38 | 0.17 |
表1-藤黄微球菌在存在1-4%羽毛的培养物中的最大角蛋白酶和蛋白酶活性以及角蛋白水解产物浓度。
对不同角蛋白底物的角蛋白分解潜力
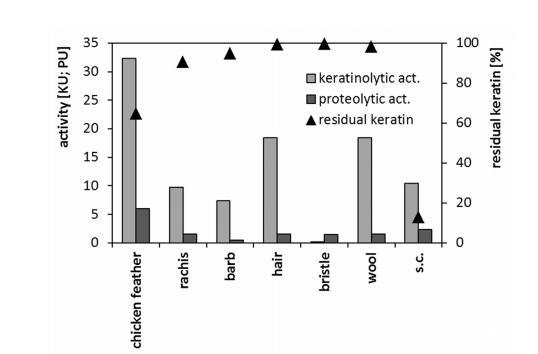
藤黄微球菌B1pz菌株除了能够有效分解鸡羽毛底物外,还能在各种角蛋白材料存在下生长和生产角蛋白酶。在人发或羔羊毛上培养物中观察到的最大角蛋白分解活性水平,与鸡羽毛培养基相比降低了约50%(图4)。分离的鸵鸟羽毛羽轴和羽枝被证明是效果差得多的角蛋白酶诱导物,而在含有猪鬃的培养基中未检测到角蛋白酶活性。测试的菌株在鸡羽毛上生长时优先产生角蛋白分解酶,而不是在其他高弹性的"硬角蛋白"上,这也反映了在短短4天培养期内底物分解程度达到35.3%。表皮角质层作为富含细胞角蛋白的"软"角蛋白的例子,尽管对细菌生物降解具有高度敏感性,但对测试菌株来说仍然是一个中等强度的角蛋白酶诱导物。
粗培养液中角蛋白酶和蛋白酶的初步表征
粗培养液中的角蛋白酶和蛋白酶分别在pH 9.4、55°C和pH 8.6、45°C下表现出总体最佳活性。使用特异性蛋白酶抑制剂的分析揭示了丝氨酸蛋白酶的主导存在,这是由于对PMSF的高敏感性,这指的是对酪蛋白和可溶性角蛋白的活性。然而,硫醇依赖性蛋白酶的显著组成部分是高度可能的,这通过半胱氨酸的激活和对NEM的敏感性得到验证。在EDTA存在下角蛋白分解活性的降低,连同Ca²⁺的巨大激活,可能表明测试的培养液中存在金属蛋白酶或其他金属依赖性蛋白酶(表2)。无细胞粗培养液中的角蛋白酶对天然羽毛角蛋白表现出活性,很大程度上受CaCl₂添加的影响(数据未显示)。在CaCl₂0.5 mM存在下,其为9.8±0.2 KU/h(对应的在没有CaCl₂的可溶性角蛋白上的活性:.3 KU)。
| 抑制剂/激活剂 | 浓度[mM] | 残余活性[%] | |
| 角蛋白分解活性 | PMSF | 10 | 28 |
| EDTA | 5 | 100 | |
| 10 | 30 | ||
| NEM | 10 | 0 | |
| Cys | 1 | 164 | |
| Ca²⁺ | 5 | 1606 | |
| 蛋白水解活性 | PMSF | 10 | 0 |
| EDTA | 5 | 100 | |
| 10 | 100 | ||
| NEM | 5 | 86 | |
| 10 | 23 | ||
| Cys | 1 | 586 | |
| Ca²⁺ | 10 | 814 |
表2-抑制剂和激活剂对藤黄微球菌B1pz粗培养液中角蛋白酶和蛋白酶活性的影响。
相关新闻推荐
2、生长曲线分析揭示:戈登氏链球菌通过ManL非特异性CCR机制抗衡致病菌(四)
