1.2实验方法
1.2.1鳜鱼蛋白水解物的制备
取新鲜鳜鱼肉搅成鱼糜,与石油醚按1∶1(g∶mL)的料液比混合,并于40℃慢摇脱脂16 h。收集沉淀鱼糜进行真空干燥后,加去离子水制成底物浓度为10%的混合物,按0.2%的比例加入风味蛋白酶,调节pH为7.0,于50℃水浴恒温振荡3 h后,90℃水浴灭酶10 min。酶解物经离心(8 000 r/min,15 min,4℃)后取上清液进行冷冻干燥,-20℃保存,备用。
1.2.2鳜鱼多肽-锌螯合物的制备
取冷冻干燥后的酶解粉用去离子水溶解(40 mg/mL),按一定比例加入80 mg/mL的ZnSO4·7H2O溶液,用NaOH和HCl调节pH为6.0,30℃水浴恒温振荡1 h。反应结束后,将反应液放置室温下冷却,离心(8 000×g,15 min),获得上清液(S1)和沉淀物(P1)。在S1中加入无水乙醇至体积分数为80%,在4℃条件下静置1 h后离心(8 000×g,15 min),得到上清液(S2)和沉淀物(P2),方法记作“离心-醇沉法”。将反应液与乙醇直接按比例混合,然后离心(8 000×g,15 min),分离上清液(S3)和沉淀(P3),方法记作“醇沉-离心法”。在蛋白质利用率方面,S1=S2+P2;P3=P1+P2。收集螯合物P1、P2和P3,冷冻干燥后-20℃保存,备用。
1.2.3菌悬液的制备
挑取活化后的腐生葡萄球菌单菌落接种于LB液体培养基中,37℃摇床培养16 h,用灭菌生理盐水将其配制成含菌数106 CFU/mL的菌悬液,现配现用。
1.2.4抑菌圈
测定鳜鱼多肽-锌螯合物对腐生葡萄球菌的抑菌圈。吸取腐生葡萄球菌菌悬液50μL于无菌培养皿中,取15 mL融化的LB固体培养基至含有菌悬液的培养皿中,混合均匀,待冷却凝固,将牛津杯固定于培养基表面。取50 mg/mL的螯合物溶液200μL于牛津杯中,以加无菌水和酶解液为对照组,做3组平行试验。37℃条件下培养24 h后用游标卡尺测量抑菌圈的直径,按照抑菌圈直径大小进行敏感性评判。
1.2.5最小抑菌浓度
将多肽-锌螯合物溶解于无菌LB培养液中并进行二倍稀释,使得最终质量浓度分别为25、12.5、6.25、3.12、1.56、0.78、0.39、0.19 mg/mL,依次加入等体积的腐生葡萄球菌菌悬液,以不加菌悬液的为对照组,做3组平行试验。37℃、150 r/min摇床培养24 h后,测量在600 nm波长处的吸光值。
1.2.6生长曲线
将腐生葡萄球菌菌悬液按1%接种量加至LB液体培养基中,以加入MIC、0.5 MIC和0.25 MIC的鳜鱼多肽-锌螯合物为实验组,以不加螯合物的为对照,做3组平行试验。37℃、150 r/min摇床培养24 h。每隔2 h取样测量在600 nm波长处的吸光值,绘制腐生葡萄球菌生长曲线。
1.2.7电导率值
将鳜鱼多肽-锌螯合物分别加入到腐生葡萄球菌菌悬液中,使得终浓度为MIC和0.5 MIC,并以未加螯合物的为对照,做3组平行试验。37℃、150 r/min摇床培养8 h,每隔2 h取样离心(4℃、8 000 r/min、15 min),取上清液,适当稀释后测定培养液电导率。
1.2.8紫外吸收值
将鳜鱼多肽-锌螯合物分别加入到腐生葡萄球菌菌悬液中,使得终浓度为MIC和0.5 MIC,并以未加螯合物的为对照,做3组平行试验。37℃,150 r/min摇床培养8 h,每隔2 h取样用0.22μm的滤膜过滤,分别检测滤液在260 nm和280 nm波长处的吸光值。
1.2.9超氧化物歧化酶和过氧化氢酶活力
将鳜鱼多肽-锌螯合物分别加入到腐生葡萄球菌菌悬液中,使得终浓度为MIC、0.5 MIC,以未加螯合物的为空白对照,做3组平行试验。37℃,180 r/min摇床培养,定时取样,低温超声2 min,离心(4℃、5 000 r/min、15 min)后取上清液,按试剂盒方法测定SOD和CAT活力。
1.2.10生物扫描电子显微镜(scanning electron microscope,SEM)
将鳜鱼多肽-锌螯合物分别加入到腐生葡萄球菌菌悬液中,使得终浓度为MIC和0.5 MIC,并以未加螯合物的为空白对照,37℃,150 r/min摇床培养15 h。培养物经离心(4℃、4 000 r/min、10 min)后收集沉淀,用磷酸缓冲液(0.2 mol/L pH 7.0)清洗2次,去上清液,用2.5%(体积分数)戊二醛固定液固定样本,4℃过夜放置。倒出戊二醛溶液,用磷酸缓冲液(0.1 mol/L,pH 7.0)漂洗菌体样品3次,每次15 min;用1%(体积分数)的锇酸溶液固定样品1~2 h;倒出锇酸废液,用磷酸缓冲液(0.1 mol/L,pH 7.0)漂洗菌体样品3次,每次15 min;再分别用30%、50%、70%、80%、90%和95%的乙醇溶液对菌体样品逐级脱水,每种浓度均处理15 min,以上操作均在4℃条件下进行。在常温下,再用100%的乙醇继续脱水2次,每次20 min。接着用乙醇与醋酸异戊酯的混合液(体积比1∶1)处理样品30 min,再用纯醋酸异戊酯处理样品。临界点干燥,镀膜后使用扫描电镜观察拍照。
1.3数据统计与分析
实验数据均采用平均值±标准偏差表示,采用SPSS 16.0软件进行数据统计与分析,多组间数据使用单因素方差分析,Duncan’s检验与LSD法均值多重比较;P<0.05表示存在统计学显著差异;使用Origin 2018作图。
2结果与分析
2.1抑菌圈
通过牛津杯法分别测试了P1、P2和P3对腐生葡萄球菌的抑菌圈及直径,如图1和表1所示。由图1可知,鳜鱼肉酶解液对腐生葡萄球菌无抑菌效果;3种多肽-锌螯合物对腐生葡萄球菌均有一定的抑菌活性,推测鳜鱼多肽-锌螯合物的抑菌活性可能与锌离子有关。其中P3的抑菌效果最好,抑菌圈直径达到(21.39±2.46)mm,其次是P2,抑菌圈直径大小为(17.89±3.06)mm,P1抑菌圈直径<10 mm,对腐生葡萄球菌有低敏感度。张钰源采用滤纸片法测定大鲵肽与大鲵肽-锌螯合物对金黄色葡萄球菌、腐败希瓦氏菌、大肠杆菌、产气肠杆菌、枯草芽孢杆菌和变形杆菌的抑菌效果,发现大鲵肽对6种菌没有抑菌活性,而大鲵肽-锌螯合物对6种菌均有抑菌活性,研究结果与本实验结论相似。由于P1的抑菌敏感度较低,后续将重点研究P2和P3的抑菌机制。

表1鳜鱼多肽-锌螯合物对腐生葡萄球菌的抑菌圈直径
注:抑菌圈直径<10 mm:低敏感或无效,用-代表;10 mm≤抑菌圈直径<15 mm:中敏感,用+代表;15 mm≤抑菌圈直径<20 mm:高敏感,用++代表;抑菌圈直径≥20 mm:极敏感,用+++代表。
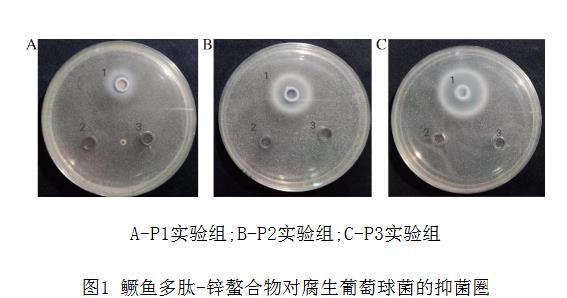
A-P1实验组;B-P2实验组;C-P3实验组
图1鳜鱼多肽-锌螯合物对腐生葡萄球菌的抑菌圈
注:1、2、3分别表示螯合物、酶解液、无菌水。
相关新闻推荐
1、活性酵母与酵母培养物饲喂育肥牛生长性能、胴体指标和牛肉品质的比较
