研究简介
本研究聚焦于III-E型CRISPR-Cas系统,首次系统揭示了其效应复合物Craspase的结构、激活机制及独特的免疫防御策略。III-E型系统与其他经典III型系统的关键区别在于缺乏标志性的Cas10蛋白,其效应蛋白gRAMP与一个TPR-CHAT肽酶结合形成Craspase复合物,但其结构特征与免疫机制此前未知。研究团队通过冷冻电镜解析了来自Candidatus “Scalindua brodae”的gRAMP-crRNA、gRAMP-crRNA-靶RNA(TR)复合物,以及Craspase分别结合同源靶RNA(CTR,其3‘端反标签序列与crRNA的5’标签不互补)或非同源靶RNA(NTR,其3‘端反标签序列与crRNA的5’标签互补)等多种状态的高分辨率结构。结构分析发现,gRAMP由四个Cas7样结构域(Cas7.1-Cas7.4)和一个Cas11样结构域融合而成,包裹着crRNA。
重要的是,研究阐明了gRAMP切割靶RNA的分子机制,鉴定出Cas7.2结构域的D547和Cas7.3结构域的D698/D806分别是两个切割位点的关键催化残基。本研究的核心发现是,Craspase的蛋白酶活性受到靶RNA的严格调控。当CTR(其3‘反标签与crRNA的5’标签不互补)结合时,其3‘反标签会结合到Craspase中TPR-CHAT结构域的一个独特通道,引发TPR-CHAT发生显著的构象变化,从而变构激活其蛋白酶活性。被激活的TPR-CHAT会特异性切割一个附属蛋白Csx30(切割位点为L407之后)。
功能实验表明,这种切割触发了流产感染(abortive infection)的细胞死亡过程,构成了III-E型系统的抗病毒策略。该过程需要另外两个蛋白Csx31和Sigma因子SbRpoE的参与。突变TPR-CHAT的催化位点(H585/C627)或Csx30的切割位点(L407A)都会显著削弱抗噬菌体防御能力。相反NTR或仅含互补序列的TR结合则无法激活该蛋白酶活性。该研究首次完整揭示了III-E型CRISPR-Cas系统不依赖于Cas10、而是通过靶RNA调控的蛋白酶活性来执行免疫防御的全新机制,为理解CRISPR-Cas系统的多样性以及开发新的RNA靶向工具提供了重要的结构基础和理论依据。
Bioscreen 全自动生长曲线分析仪的应用
Bioscreen C全自动微生物生长曲线分析仪被用于细菌生长实验,以评估III-E型CRISPR-Cas系统的抗病毒效果。研究人员将携带编码gRAMP-crRNA、TPR-CHAT以及Csx30-Csx31-SbRpoE蛋白复合物质粒的大肠杆菌(实验组)与携带空载体的对照菌株,分别接种于补充抗生素的LB培养基中,并加入不同感染复数(MOI为4和0.1)的λ噬菌体裂解液或缓冲液对照。该设备通过实时、高通量地监测96孔板或100孔板中细菌培养物的光密度(OD600 nm)变化,自动绘制生长曲线,从而精确量化细菌在噬菌体感染下的存活与生长抑制情况。实验结果表明当Craspase系统被同源靶RNA(CTR)激活并切割Csx30蛋白后,会触发流产感染(abortive infection)的细胞死亡程序,导致细菌生长受到显著抑制。而突变失活该系统则削弱了这种抗病毒防御能力。 。
实验结果
III-E型CRISPR-Cas系统采用了一种全新的免疫防御机制。该机制的核心是其效应复合物Craspase,它由gRAMP蛋白与TPR-CHAT肽酶组成。研究发现,只有当同源靶RNA(其3‘端序列与crRNA的5’标签不互补)结合Craspase时,才会诱导TPR-CHAT发生显著的构象变化,从而变构激活其蛋白酶活性。被激活的蛋白酶进而特异性切割附属蛋白Csx30,该切割事件在Csx31和Sigma因子SbRpoE的参与下,最终触发细菌的流产感染(程序性细胞死亡),以此作为限制病毒传播的抗病毒策略。这一工作完整揭示了III-E型系统不依赖于经典Cas10蛋白,而是通过RNA指导的蛋白酶激活来执行免疫功能的独特途径。
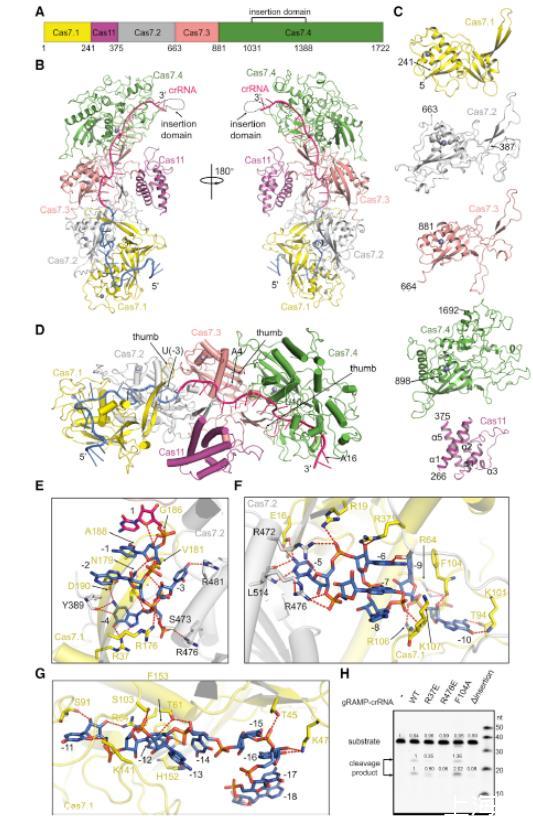
图1、 gRAMP-crRNA的冷冻电镜结构。(A)布罗德氏斯卡林多菌中 gRAMP的结构域组成。Cas7.1–7.4 与 Cas11 结构域分别以品红色、黄色、灰色、粉色与绿色标示。(B)gRAMP-crRNA 的整体结构。gRAMP 结构域着色同(A);crRNA的间隔区与重复区分别以亮粉色与海蓝色标示。Cas7.4内未建模的插入片段已标注。(C)gRAMP各独立结构域的结构。已标注Cas11 结构域的二级结构。(D)crRNA结合方式的特写。已标注Cas7.1–7.3结构域的拇指区域与crRNA中发生扭折的核苷酸。(E–G)gRAMP 的Cas7.1/7.2结构域分别与 crRNA第(1)–(4) 位核苷酸(E)、第 (5)–(10) 位核苷酸(F)、第(11)–(18)位核苷酸(G)的相互作用。红色虚线代表极性相互作用。(H)gRAMP-crRNA及其突变体对靶标RNA的切割。Δ插入片段表示缺失插入片段(残基1031–1388)并以GSG(甘氨酸-丝氨酸-甘氨酸)连接子替代的gRAMP-crRNA。
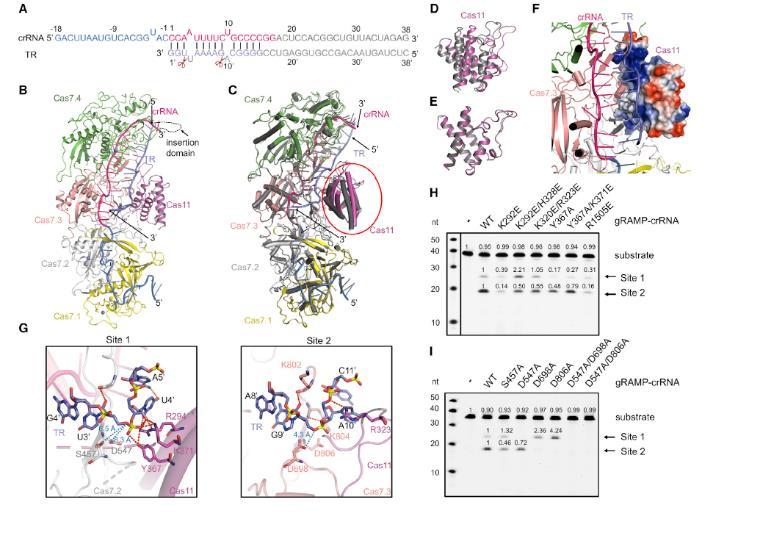
图 2、gRAMP-crRNA - 靶标 RNA 的结构与 RNA 切割机制。(A)crRNA - 靶标 RNA 双链的示意图。实验所用 crRNA 与靶标 RNA 的核苷酸以线条表示。靶标 RNA 以深蓝色标示。结构中已建模的核苷酸如图所示;不可见核苷酸以灰色标示。剪刀代表切割位点。(B)gRAMP-crRNA - 靶标 RNA 的整体结构。靶标 RNA 着色同(A)。(C)gRAMP-crRNA(深灰色)与 gRAMP-crRNA - 靶标 RNA(着色同 B)的结构叠加。Cas11 结构域区域以圆圈突出显示。(D)(C)中结构叠加后 Cas11 结构域区域的特写。(E)gRAMP-crRNA 与 gRAMP-crRNA - 靶标 RNA 中独立 Cas11 结构域的结构比对。(F)gRAMP-crRNA - 靶标 RNA 结构中 Cas11 区域的特写,Cas11 结构域以静电势模型着色。(G)gRAMP 与靶标 RNA 在两个切割位点的详细相互作用。红色虚线代表极性相互作用。(H)gRAMP-crRNA 及其破坏间隔区靶标 RNA 结合的突变体对靶标 RNA 的切割。已标注代表位点 1 与位点 2 切割的产物条带。(I)gRAMP-crRNA 及其两个切割活性位点突变体对靶标 RNA 的切割。
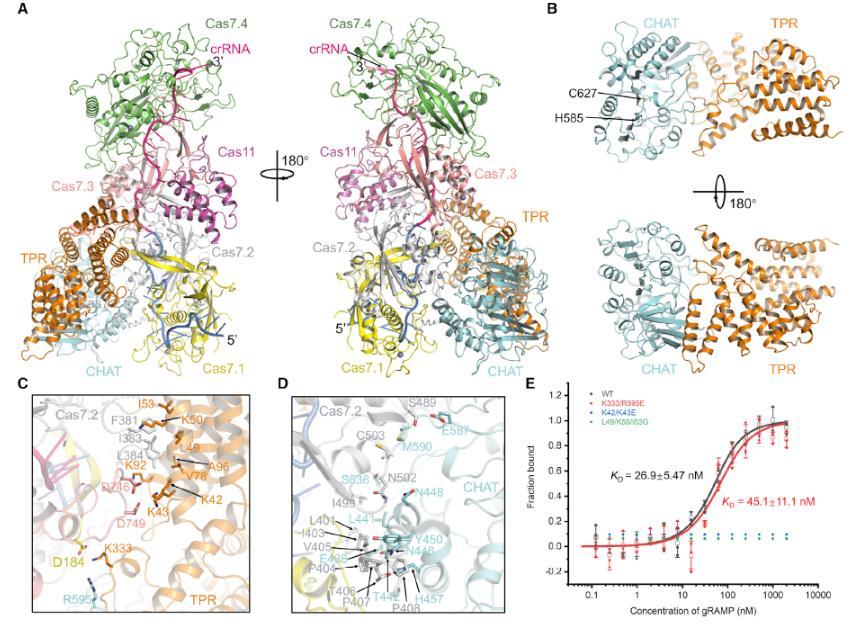
图 3 、Craspase 的冷冻电镜结构。(A)Craspase 的整体结构。gRAMP-crRNA 着色同图 1B;TPR-CHAT 的 TPR 与 CHAT 结构域分别以橙色与青色标示。(B)Craspase 中 TPR-CHAT 的整体结构,着色同(A)。两个活性位点残基以球棍模型显示。(C 与 D)gRAMP 分别与 TPR-CHAT 的 TPR 结构域(C)、CHAT 结构域(D)的详细相互作用。(E)gRAMP-crRNA 与 TPR-CHAT 及其突变体结合的微量热泳动实验。展示三次独立实验的单个数值;同时展示结合曲线与解离常数值。误差线表示三次独立实验的标准差。
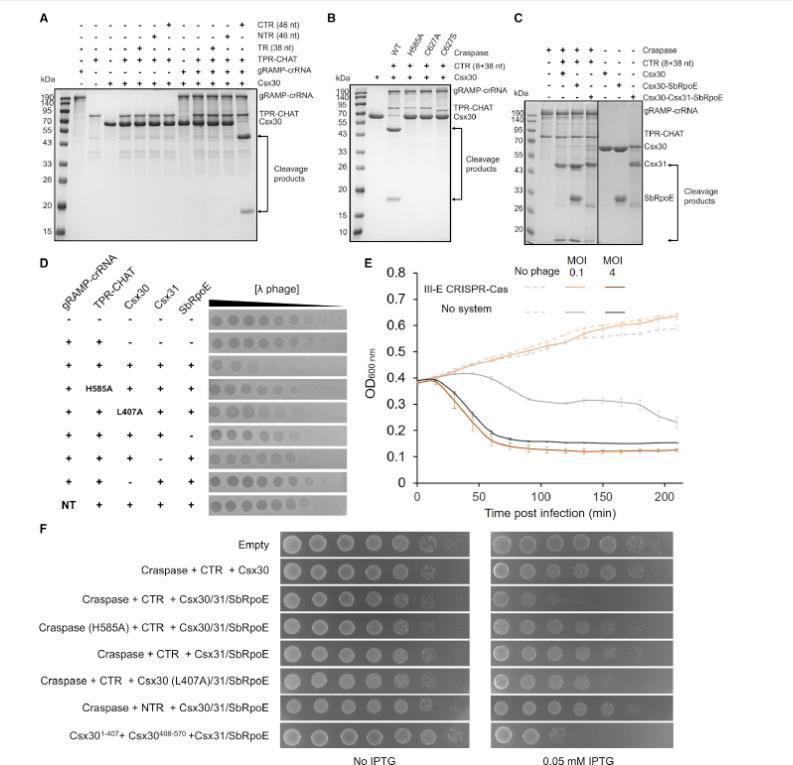
图 4、 III-E 型 CRISPR-Cas 系统的免疫机制。(A)Craspase 复合物中 TPR-CHAT 对 Csx30 的靶标 RNA 依赖性切割。分别加入 0.5μM 靶标 RNA / 非互补靶标 RNA / 互补靶标 RNA、0.3μM TPR-CHAT、0.3μM gRAMP-crRNA 与 1.5μM Csx30。(B 与 C)Craspase 或其 TPR-CHAT 活性位点突变体对 Csx30 的靶标 RNA 依赖性切割。(D)III-E 型 CRISPR-Cas 操纵子抵御噬菌体。展示 λ 噬菌体在表达布罗德氏斯卡林多菌 III-E 型 CRISPR-Cas 操纵子基因的大肠杆菌 BL21 (DE3) 细胞上的铺板效率。实验独立重复三次,展示代表性结果。NT,非靶向。(E)表达 III-E 型 CRISPR-Cas 操纵子五种基因的大肠杆菌细胞或对照大肠杆菌细胞(无系统)的液体培养物生长。细胞在 37℃被 λ 噬菌体感染。时间 0 时以感染复数 4 或 0.1 感染细菌。每个感染复数设置三次生物学重复,误差线为平均值 ± 标准差。(F)III-E型 CRISPR-Cas 系统的激活具有细胞毒性。编码所示质粒的细胞在无诱导或诱导表达条件下,在 LB 琼脂上进行 10 倍梯度稀释点板。
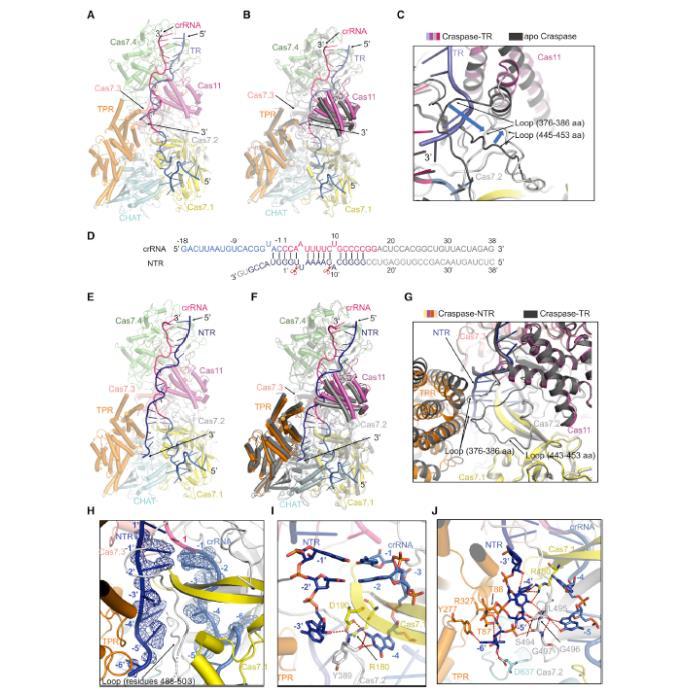
图5 、Craspase-靶标RNA与Craspase-非互补靶标RNA的冷冻电镜结构(A)Craspase (着色同图 3A)结合靶标 RNA(深蓝色)的整体结构。(B)Craspase(深灰色)与 Craspase - 靶标 RNA(着色同 A)的结构叠加。(C)(B)中结构叠加后 Cas11 结构域邻近两个环区域的特写。Craspase 与 Craspase - 靶标 RNA 着色同(B)。(D)Craspase - 非互补靶标 RNA 中 crRNA - 非互补靶标 RNA 双链的示意图。实验所用 crRNA 与非互补靶标 RNA 的核苷酸以线条表示。非互补靶标 RNA 以深蓝色标示。不可见核苷酸以灰色标示。(E)Craspase(着色同图 3A)结合非互补靶标 RNA(深蓝色)的整体结构。(F)Craspase(深灰色)与 Craspase - 非互补靶标 RNA(着色同 E)的结构叠加。(G)Craspase - 非互补靶标 RNA(着色同 E)与 Craspase - 靶标 RNA(深灰色)结构叠加后所示两个环区域的特写。注:Craspase - 非互补靶标 RNA 结构中残基 443–453 环区域无序。(H)非互补靶标 RNA 的 3' 抗标签区可建模 6 个核苷酸。Craspase - 非互补靶标 RNA 着色同(E)。非互补靶标 RNA 第 (1)'–(6)' 位与 crRNA 第 (1)–(6) 位核苷酸对应的电子云密度以网格显示。(I 与 J)Craspase 分别与非互补靶标 RNA 第 (1)'–(3)' 位(I)、第 (4)'–(6)' 位(J)核苷酸的详细相互作用。
总结
在III-E型CRISPR-Cas系统中,Cas效应蛋白(gRAMP)与TPR-CHAT结合形成Craspase (CRISPR引导的半胱天冬酶)。然而该系统中gRAMP的结构特征和免疫机制尚不清楚。本研究解析了gRAMP-crRNA、gRAMP:cRNA:靶标RNA的结构,以及Craspase、Craspase结合互补靶标RNA(CTR)或非互补靶标RNA(NTR)的复合物结构。重要的是NTR和CTR的3'抗标签区结合在Craspase的两个不同通道,带有非互补3'抗标签的CTR诱导TPR-CHAT发生显著构象变化,通过别构效应激活其蛋白酶活性以切割辅助蛋白Csx30。该切割随后触发流产性感染,作为III-E型系统的抗病毒策略。
本研究为gRAMP的催化机制和III-E型系统的免疫机制提供了关键见解。Bioscreen C全自动微生物生长曲线分析仪,通过实时、高通量监测细菌培养物在600 nm波长下的光密度(OD)变化,绘制生长动力学曲线,以评估III-E型CRISPR-Cas系统的抗病毒功能。Bioscreen提供的实时生长曲线数据,直观且定量地证实了该CRISPR系统通过触发细胞死亡程序来执行抗病毒防御的生物学机制。
相关新闻推荐
2、溶藻弧菌噬菌体φV039C一步生长曲线等生物学特性的研究——摘要、材料与方法
