最优杂交菌株的评估
葡萄糖-D-木糖混合物的发酵性能
三个选定菌株GSE16(通过GS1.11-26与Ethanol Red分离株回交获得)、GSF335和GSF767(通过GS1.11-26与JT21653分离株杂交获得)在更可控的发酵实验中进行评估,在100毫升YP培养基中含有36克/升葡萄糖和37克/升D-木糖,35°C。接种物细胞密度为1.3克干重/升。三个杂交菌株的性能与之前报道的菌株GS1.11-26进行比较。GS1.11-26在大约13小时内完全消耗D-木糖和葡萄糖,而其他三个菌株需要大约32小时。
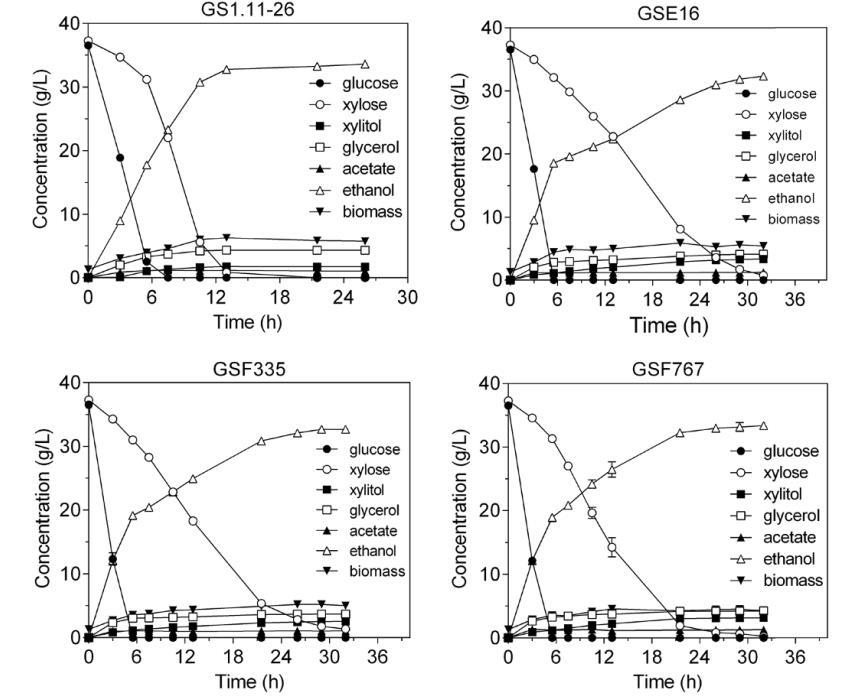
图9 三种新杂交菌株与GS1.11-26在葡萄糖和D-木糖混合物中发酵性能的比较。发酵在含有37克/升葡萄糖和37克/升D-木糖的YP培养基中进行,初始生物量为1.3克/升。误差棒代表两次实验平均值的标准偏差。
三个新杂交菌株的葡萄糖消耗速率高于进化菌株GS1.11-26。此外,GSF335甚至显示出比原始亲本菌株HDY.GUF5略高的葡萄糖消耗速率。然而,GS1.26在D-木糖消耗速率和D-木糖乙醇生产力方面仍然优越。在三个新杂交菌株中,GSF767显示出最高的D-木糖消耗速率(0.65克/克干重/小时),但其最大D-木糖利用速率仍比GS1.11-26(1.10克/克干重/小时)低约40%。另一方面,GS1.11-26和GSF767获得了相同的乙醇产量(0.46克/克初始糖或理论最大值的90.2%),而其他两个菌株GSF335和GSE16的产量略低(0.44克/克初始糖或理论最大值的86.3%)。所有三个新杂交菌株以及GS1.11-26都观察到D-木糖和葡萄糖的部分共利用,如前所述。
富含抑制剂的云杉水解物中的发酵性能
三个新杂交菌株GSE16、GSF335和GSF767在酸预处理云杉材料的发酵实验中评估抑制剂耐受性。使用云杉材料的全浆液60%,补充酵母提取物和蛋白胨。添加了葡萄糖(40克/升),因为水解物中的糖浓度相当低(约13克/升),这将不允许菌株之间发酵性能的适当比较。在这些条件下,GSF335和GSE16的发酵速率(从CO2释放估计)比GS1.11-26快得多。GSF767也表现略好于GS1.11-26。这一结果表明,新杂交菌株特别是GSF335和GSE16,对酸预处理云杉水解物中存在的抑制剂具有显著更好的耐受性。
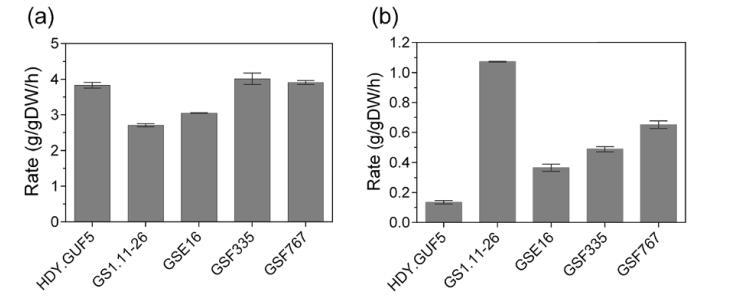
图10 三种新杂交菌株和GS1.11-26达到的最大糖消耗速率。(a)最大葡萄糖消耗速率;(b)最大D-木糖消耗速率。数值来自图9所示的发酵实验。最大D-木糖利用速率在葡萄糖耗尽后获得。误差棒代表两次实验平均值的标准偏差。
为了更精确地评估云杉水解物中的D-木糖和葡萄糖利用速率,我们在类似的批次发酵中研究了三个菌株的性能,使用固体负荷为11%(对应于约50%浆液)的未脱毒云杉水解物,并补充葡萄糖和D-木糖至终浓度分别为62克/升和18克/升。发酵在初始细胞密度为4克干重/升时进行。所有三个菌株以及对照菌株HDY.GUF5和GS1.11-26在不到10小时内完全消耗了葡萄糖和甘露糖(来自水解物),GSF767显示出最快的葡萄糖消耗速率,在4小时内使用了所有葡萄糖。D-木糖发酵速率比葡萄糖发酵慢得多,现在对于所有菌株来说比在更浓的水解物中更为相似(除了HDY.GUF5,它不能使用D-木糖)。杂交菌株GSF767显示出与GS1.11-26相似的D-木糖发酵速率,而GSE16和GSF335的速率略低。三个杂交菌株和GS1.11-26没有产生木糖醇,只产生少量甘油(约0.05克/克)。尽管D-木糖利用速率较慢,但杂交菌株和GS1.11-26获得的最终乙醇浓度和产量是可比的。与HDY.GUF5相比,两个杂交菌株GSE16和GSF767以及GS1.11-26产生的乙醇多约23%,因为它们有效地利用了D-木糖。GSF335的乙醇产量较低,但仍比HDY.GUF5高13%。
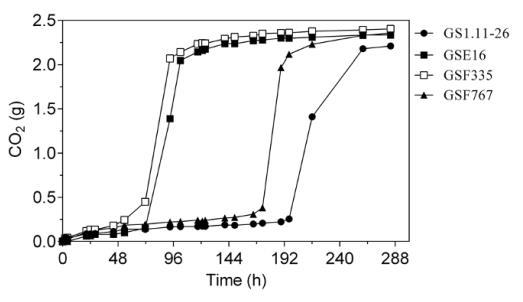
图11 小规模发酵实验中三种新杂交菌株在酸预处理云杉水解物中的抑制剂耐受性测定。发酵使用补充40克/升葡萄糖的云杉水解物全浆液(60%)进行,连续搅拌200转/分钟。细胞以1.3克干重/升的初始细胞密度从稳定期预培养物接种到YP培养基中。发酵过程中通过重量损失估算CO2产生。
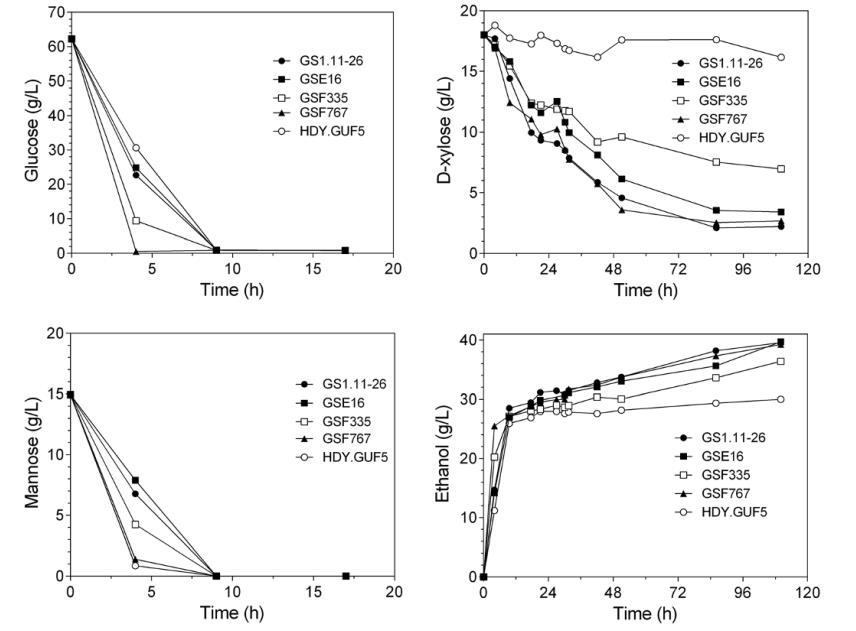
图12 三种新杂交菌株在半厌氧批次发酵中使用酸预处理云杉水解物的发酵曲线。发酵使用固体负荷为11%的酸预处理云杉水解物进行,补充酵母氮基、硫酸铵和氨基酸。最终葡萄糖和D-木糖浓度分别调整为62克/升和18克/升。甘露糖仅来自水解物。发酵在初始密度为4克干重/升时开始,连续搅拌200转/分钟。
超高浓度发酵中的发酵性能
杂交菌株GSE16、GSF335和GSF767还使用含有330克/升葡萄糖的YP培养基评估了超高浓度发酵中的发酵性能。野生型HDY.GUF5和进化菌株GS1.11-26作为对照包括在内。发酵在连续搅拌120转/分钟和主要静态条件下进行,仅在开始时搅拌4小时。在这两种条件下,三个杂交菌株的表现都比GS1.11-26好得多。
在连续搅拌下,GSF335显示出最快的发酵速率。它达到了与HDY.GUF5相同的最终乙醇浓度,但大约早96小时。此外,GSF335在静态发酵条件下也显示出最快的发酵速率。然而,在静态条件下达到的最高最终乙醇浓度是由GSE16达到的。GSF767在发酵速率方面与HDY.GUF5相似,但在两种条件下达到的最终乙醇浓度略低。总体而言,三个杂交菌株在静态和连续搅拌条件下都比GS1.11-26表现好得多。GSF335在搅拌发酵条件下表现出优异的性能,仅在72小时内积累了最高的乙醇浓度。在单独的超高浓度发酵实验中,GSF335积累的最终乙醇浓度高于四倍体菌株GS1.11-26/Fseg25和二倍体菌株Fseg25。
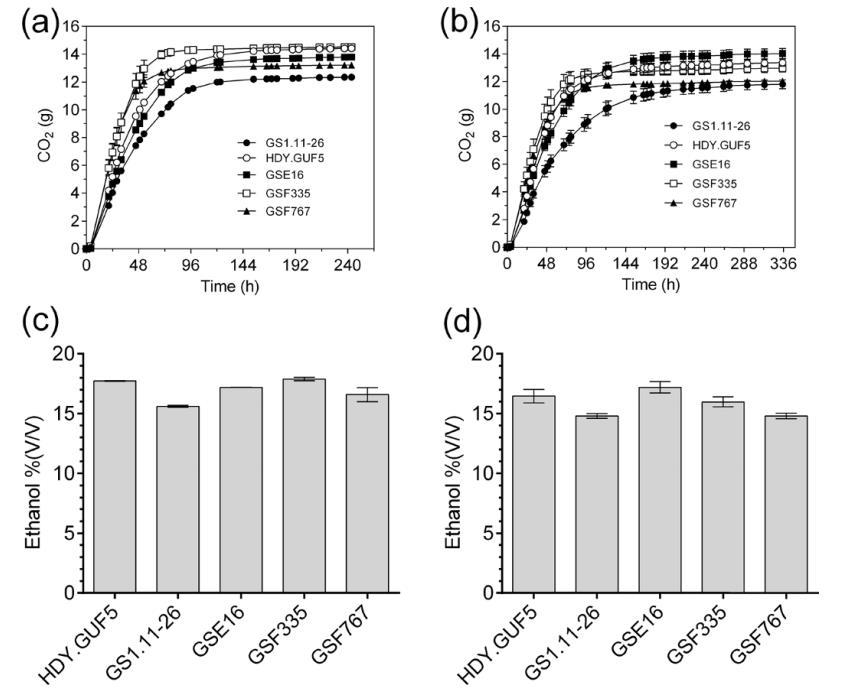
图13 含有330克/升葡萄糖的YP培养基中的超高浓度发酵。(a)和(b)分别显示连续搅拌和静态条件下的发酵曲线。(c)和(d)中的图显示(a)和(b)发酵过程中产生的最终乙醇浓度。发酵在初始细胞密度为1.3克干重/升时开始。
讨论
本论文的目标是开发一种优良的D-木糖利用工业酵母菌株,缺乏先前报道的菌株GS1.11-26背景中在诱变和/或进化工程过程中引入的负面特性。GS1.11-26菌株的开发表明,在工业酵母菌株中引入高效的D-木糖发酵能力需要多重遗传修饰。因此,与胁迫和抑制剂耐受性一样,高效的D-木糖发酵是一种多基因性状,工程化此类性状以开发优良工业酵母菌株一直是理性工程策略的主要挑战。因此,到目前为止,该领域的大多数进展都是通过无偏方法实现的,如诱变、选择和进化工程,其中负责性能改善的潜在遗传变化通常仍然未知。
在本研究中,我们描述了三种强健工业酵母菌株的构建,它们将高效的D-木糖发酵与非常高的抑制剂耐受性相结合。这是通过结合多种策略实现的。我们将工业菌株单倍体衍生物的经典育种扩展为与交配位点纯合的二倍体菌株的育种。这使减数分裂重组的遗传库加倍。此外,我们评估了大量分离株阵列,使用多步选择程序,首先旨在通过简单的高通量测试淘汰真正差的菌株,并逐渐将选择转移到尽可能接近真实工业条件的环境中。此外,我们将候选菌株提交给非常严格的独立评估测试,例如在半厌氧超高浓度发酵中积累非常高浓度乙醇的能力。这是优良生物乙醇生产菌株的严格质量标准。
我们使用减数分裂重组来组合D-木糖利用菌株GS1.11-26和高度抑制剂耐受性菌株JT21653基因组中的优良元素。后者菌株是通过使用未脱毒酸预处理云杉水解物筛选各种来源的酵母菌株集合而确定的。我们选择这种材料是因为据报道它是抑制剂最多的水解物之一,含有多种抑制剂,包括糠醛衍生物糠醛和HMF、脂肪族酸如乙酸、甲酸和乙酰丙酸,以及各种酚类化合物如香草酸、香草醛、丁香醛、丁香酸和4-羟基苯甲酸。耐受这种培养基的菌株很可能也耐受以较不严格方式预处理的其他木质纤维素水解物中的抑制剂。此外,基于酸的热化学预处理被认为是木质纤维素原料生物转化为液体生物燃料生产中最具成本竞争力的预处理方法之一。因此,预计此类菌株具有广泛的应用前景。
相关新闻推荐
2、不同浓度冠菌素对番茄防御基因表达、胼胝质沉积及野生型致病菌生长的影响(四)
3、生长曲线分析仪操作实例:通过老化细胞的生长来量化酵母的时序寿命
