图8揭示了所描述的所有多形汉逊酵母克隆在18小时时计算出的比产物产率(标准:所有克隆已进入稳定期)。图8的整个条形图描绘了所有克隆,而放大的条形图呈现了十个最佳克隆(TOP10)。条形图揭示了比产物产率的巨大多样性,因此需要进行复杂的筛选。
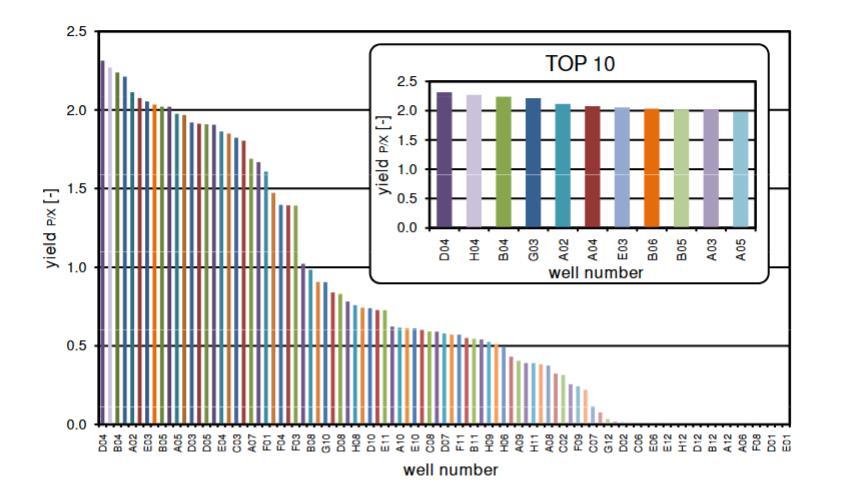
图8:比产物产率(Yp/x)的推导。数据取自图7的克隆筛选,比产物产率Yp/x计算为GFP强度(蛋白质浓度)与散射光强度(生物量浓度)的比率;数据排列从左到右呈现最佳克隆,横坐标上给出孔号,TOP10代表在YP/X方面最好的十个克隆。
生物过程的另一个评估标准可能是过程的体积生产率(Pv)。图7C可视化了微滴度板所有96孔中体积生产率的发展。体积生产率源自GFP荧光单位(FU,相当于产物浓度~mg/L)除以培养时间(净生产率,不含设置时间)。再次观察到非常多样化的曲线。所有体积生产率都达到一个峰值,此时应该收获培养物。图7C图中突出显示了最佳克隆的孔号。关于体积生产率,最明智的做法是继续用这些克隆进行生物工艺开发。最大体积生产率点反映了预期的工艺性能和最佳收获点。再次,在线测量的GFP荧光在这种情况下可以被视为一个方便的模型,但就工业实践而言,与荧光报告蛋白的融合蛋白或离线蛋白质分析可能是更现实的情况。因此,利用本文介绍的工具,在生物工艺开发的早期阶段就可以对克隆和发酵条件进行复杂的评估。
启动子表征
启动子调控是评估表达系统或生物过程时另一个非常重要的方面。目前仍难以生成关于启动子调控的有意义数据。目前应用了许多费力的技术,例如荧光显微镜或荧光激活细胞分选(FACS)。可以通过从培养容器中繁琐地取样获得启动子活性或蛋白质表达的动力学。启动子活性通常通过添加特定诱导剂或在特定底物上生长来控制。
图9展示了多形汉逊酵母启动子调控的一个示例。研究了两种不同的启动子,MOX和FMD,以及野生型菌株作为阴性对照。将两种启动子插入转化质粒中的GFP基因前面,以通过GFP的荧光跟踪启动子活性。酵母菌株在两种不同的碳源上培养,以研究葡萄糖和甘油上的启动子调控。图9清楚地描述了菌株在不同培养基上生长和启动子活性的差异。在两种碳源上,生长顺序是相同的,而野生型菌株比重组菌株生长更快。此外,这两种重组菌株以相似的生长速率生长,FMD菌株生长略快。证实了图5中的发现,所有菌株在葡萄糖上的生长速率都高于在甘油上。
在甘油上的生物量产率似乎是在葡萄糖上的两倍高(在相同摩尔质量下)。在葡萄糖上,野生型菌株在5小时,MOX和FMD菌株在大约7小时,散射光信号略有下降后,似乎存在第二个生长期。在后一阶段,细胞代谢在葡萄糖生长期间形成的溢出代谢物,乙醇和乙酸。图9的下图显示了菌株的GFP形成。在葡萄糖上,在存在葡萄糖的情况下(第一生长期),似乎根本没有启动子活性。仅在切换到第二生长期(在乙醇和乙酸上)之后,启动子被激活并形成GFP。FMD和MOX菌株以相似的浓度和相同的生长顺序形成GFP。可能也利用了培养基(YP基础)的复杂成分,如蛋白胨和酵母提取物,来形成GFP,因为没有其他底物可用,并且GFP在稳定期仍在形成。正如预期,野生型不形成任何GFP。
然而,在甘油上,启动子的行为完全不同。在生长期和存在高甘油浓度期间,启动子已经被激活并产生GFP。两种启动子的活性直到10-11小时都非常相似。在那之后,MOX启动子活性增强,而FMD启动子下降。进入稳定期后,两种启动子活性都减慢,GFP荧光保持恒定。在发酵结束时,MOX启动子的GFP荧光强度大约是FMD启动子的2.5倍,证明了在所应用的实验条件下MOX启动子的优越性。再次,野生型不形成任何GFP。
多形汉逊酵母的这种启动子调控方案在文献中也有报道,其中在葡萄糖上,MOX和FMD启动子被底物阻遏,而在甘油上,这些启动子在相对较高的底物浓度下被去阻遏。借助BioLector,可以在培养过程中定量表征不同调控条件下的启动子活性。同时,这些启动子活性可以分配到不同的生长阶段和底物摄取。
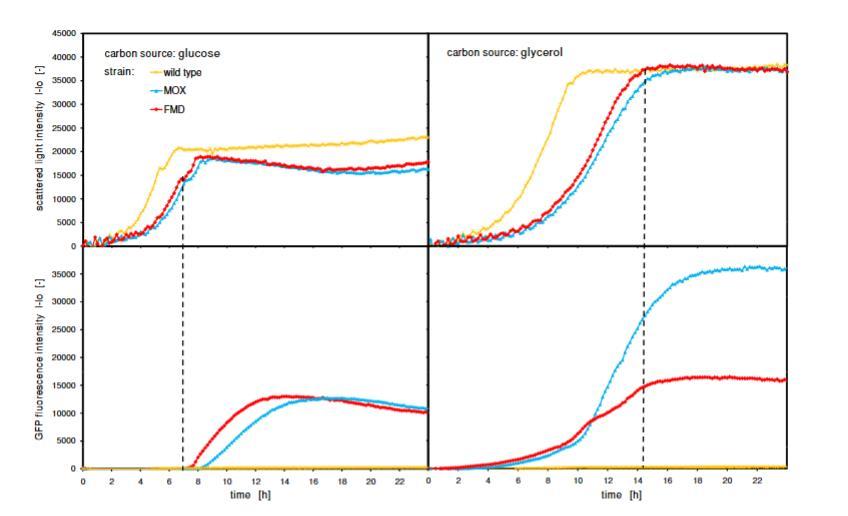
图9:启动子表征。通过GFP荧光强度和平行测量的散射光强度监测多形汉逊酵母中MOX和FMD启动子在葡萄糖和甘油生长培养基上的调控;多形汉逊酵母野生型、RB11-pC10-Mox-GFP和RB11-pC10-FMD-GFP在YPD(10 g/L葡萄糖)和YPG(20 g/L甘油)培养基中;在96孔MTP中测量,填充体积200μL,温度37°C,摇动频率995 rpm,摇动直径3 mm,散射光(激发:620 nm/发射:-,增益:20),GFP(激发:485 nm/发射:520 nm,增益:10)。
