生物量校准
需要高浓度的生物量来关联散射光强度和生物量浓度。为了达到高生物量浓度,在250 ml摇瓶中用复杂的TB和YPG培养基中培养大肠杆菌和多形汉逊酵母的野生型菌株过夜(20 mL,37°C,300 rpm,50 mm摇动直径)。通过离心(3000 rpm,5分钟,德国Hettich的Rotina 38 R)收获培养物并浓缩十倍。各取一份浓缩细胞悬浮液样品(2 mL)用于测定OD(在600 nm处的吸光度,使用分光光度计(UVIKON 922,英国Kontron Instruments))和细胞干重(CDW)。通过用生理盐水(9 g/L NaCl)洗涤细胞两次,并在105°C下将细胞干燥至质量恒定来确定CDW。然后将浓缩细胞悬浮液在相应培养培养基中的稀释液的重复样分配到新的微滴度板中,并在与培养实验相同的操作条件下用BioLector读取。OD的参考测量在微孔板吸光度读数仪(Powerwave X,美国BioTek)中进行,工作体积为200 μL,无任何覆盖,波长为600 nm。
结果与讨论
生物量校准
在生物技术实验室中,通过监测光密度来跟踪生物量发展是非常常见的。然而,众所周知,光密度与生物量浓度之间的相关性仅在非常小的范围内呈线性——通常在0.1到0.3 OD之间。因此,对于更高的生物量浓度,有必要适当稀释样品并重新计算样品的实际OD。文献中经常提到,散射光测量可以弥补这种不便,并且可以在不稀释的情况下将生物量浓度关联至高密度。为了证明这一点,比较了不同生物量浓度(CDW)的多形汉逊酵母wt在YPG培养基中的细胞悬浮液的散射光和光密度测量信号。
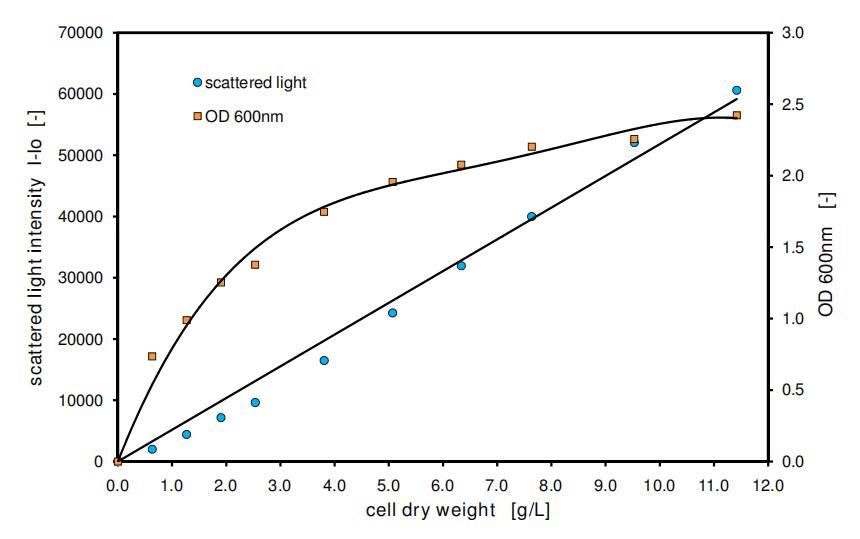
图1:散射光与光密度(吸光度)测量之间的比较。多形汉逊酵母(野生型)在YPG培养基中的培养物,在96孔MTP中测量,填充体积200μL,温度37°C,摇动频率995 rpm,摇动直径3 mm,散射光(激发:620 nm/发射:-,增益:40)。
图1显示了OD和散射光测量信号与多形汉逊酵母细胞干重浓度的相关性。OD信号遵循典型的饱和曲线,并证实线性在远低于1 g/L CDW的浓度下即已受限。然而,散射光信号显示与细胞干重浓度具有良好的线性相关性,适用于高达11 g/L CDW的应用浓度,这是在分批发酵中达到的正常浓度。此外,可以观察到散射光对生物量信号的分辨率非常高。因此,在应用的灵敏度下(增益=40),每g/L细胞干重可用5500个散射光单位来分辨。由于OD测量在生物量浓度较高时会失去分辨率,因此不建议使用此方法处理未稀释的样品。因此,该方法不适用于培养物的在线监测。
还有两个方面使得OD测量对于微滴度板中生长培养物的在线监测不切实际。首先,通常使用气体渗透膜来密封孔,以避免污染并减少蒸发。这使得透射测量几乎不可能。其次,OD测量通常在板摇动中断时进行。这导致在测量过程中细胞沉降产生测量假象。此外,对于敏感微生物或研究快速代谢反应时,必须考虑摇动中断期间氧气传质效率和混合效果的下降。
散射光测量生物量的极限
为了确定散射光测量的极限,将摇瓶培养后的大肠杆菌JM109和多形汉逊酵母wt的浓缩生物量溶液稀释,分配到微滴度板上,并用BioLector测量。结果如图2所示。
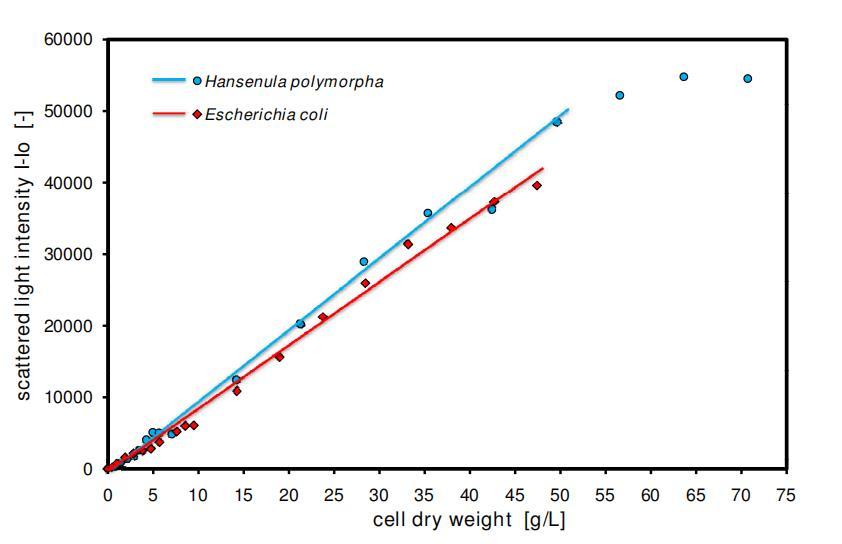
图2:散射光测量的生物量监测极限。多形汉逊酵母(野生型)在YPG培养基中;大肠杆菌JM109在TB培养基中;两者均在96孔MTP中测量,填充体积200μL,温度37°C,摇动频率995 rpm,摇动直径3 mm,散射光(激发:620 nm/发射:-,增益:5)。
在图2中,显示了稀释系列的散射光强度与细胞悬浮液细胞干重的函数关系。对于两种细胞类型,大肠杆菌和多形汉逊酵母,在广泛的浓度范围内,散射光强度与细胞干重浓度显示出良好的线性相关性。高达50 g/L细胞干重的细胞浓度,散射光强度显示与细胞干重浓度呈线性相关。在细胞浓度高于50 g/L细胞干重时,对于所描述的测量设置,多形汉逊酵母的散射光信号变得饱和。此时,分辨率急剧下降,不建议进一步监测未稀释的样品。
大肠杆菌细胞悬浮液仅跟踪到细胞干重浓度50 g/L,因为应用的摇瓶培养的生物量产率仅限于此值。然而,可以假设大肠杆菌细胞悬浮液的检测极限也在50 g/L细胞干重左右,因为直到这个浓度,酵母细胞的信号行为与细菌相似。但是,此结论不能一概而论,也不能推广到任何其他细胞类型、培养基组成或应用。为了确保可靠的测量数据,建议在使用新的细胞类型和培养基时进行特定的生物量校准。总的来说,非侵入性散射光测量反映生物量浓度的广泛线性范围和灵敏度,首次实现了在微生物反应器中在线监测细胞生长。从而避免了样品稀释、开放容器导致的污染以及摇动中断。如果接受50 g/L细胞干重作为散射光测量线性范围校准的上检测限,那么对于通常在筛选中应用的分批发酵,生物量检测显然没有限制。这种最常用的操作模式通常达到低于15 g/L的细胞干重。
对于细菌和酵母细胞,生物量浓度的最小检测限范围为0.1至0.2 g/L CDW(此处OD600 ~0.2至0.6)。当使用闪光灯作为激发光时(如本例),闪光可以在通常细胞浓度较低的培养开始时以及在未接种培养基中引起散射光信号的振荡。这是由于闪光激发光与孔内摇动液体不断变化的路径长度之间的干扰造成的。在低细胞密度或纯培养基中,光可以完全穿透液体并从覆盖微滴度板的粘性密封膜上散射回来。随着细胞密度增高,光不再能完全穿透液体,液体的路径长度对信号稳定性的影响减小。
相关新闻推荐
2、不同浓度冠菌素对番茄防御基因表达、胼胝质沉积及野生型致病菌生长的影响(四)
3、BspE 基因缺失对牛种布鲁氏菌体外生长、胞内生存、黏附能力的影响(一)
