1.2.5pH稳定性
以1mol/LHCl与1mol/LNaOH调整灭活副干酪乳杆菌Lab5CFS的pH至3、4、5、6、7、8,室温静置1h,即得到相应pH处理的灭活CFS,后调回至溶液初始pH(3.51)。控制溶液终体积一致。设未pH处理的灭活CFS组为对照组(pH3.51),以MRS液体培养基作空白参照。
1.2.6副干酪乳杆菌Lab5生长曲线的测定
副干酪乳杆菌Lab5生长曲线的测定:将副干酪乳杆菌Lab5以2%的接种量接种于MRS液体培养基,使用Bioscreen全自动生长曲线分析仪于37℃连续培养48小时,自动监测OD600nm值的变化。培养结束后,测定培养液的pH,并取发酵上清液进行抑菌实验(以MRS培养基为空白对照),测量抑菌圈直径。
1.2.7最小抑菌质量浓度(minimuminhibitoryconcentration,MIC)测定
将灭活副干酪乳杆菌Lab5 CFS冻干粉用LB肉汤配制成400 mg/mL的母液,经对半稀释,制备终质量浓度为200、100、50、25、12.5、6.25、3.125、1.5625、0.78125和0.390625 mg/mL的系列浓度溶液。分别取100 μL各浓度溶液与100 μL单增李斯特菌液(5×10⁵ CFU/mL)加入Bioscreen专用微孔板孔中。以LB肉汤与菌液混合液为阳性对照,以200 mg/mL CFS溶液与LB肉汤混合液为阴性对照。
将微孔板置于Bioscreen全自动生长曲线分析仪中,于37℃连续培养24-48小时,并自动、间歇性监测OD600nm值。通过分析生长曲线,以监测期间内与阴性对照生长无显著差异的最低药物浓度孔确定为MIC。
1.2.8副干酪乳杆菌Lab5后生元在杜黑猪肉保鲜中的应用
1.2.8.1副干酪乳杆菌Lab5后生元的制备及冷鲜猪肉的处理
副干酪乳杆菌Lab5后生元的制备:取经121℃处理25min热灭活副干酪乳杆菌Lab5CFS于真空冷冻干燥后得到后生元冻干粉备用。
以75%酒精擦拭用具后紫外照射20min,取杜黑猪背最长肌肉,剔筋去膜,切分成约150g且厚度相近肉块。设对照组(不处理)与处理组(配制2MIC、4MIC浓度副干酪乳杆菌Lab5后生元溶液并均匀涂于猪肉样品表面)置于方形塑料盒中。塑料盒用保鲜膜包裹,以确保盒内外之间的空气交换。样品放于4℃冷库,每隔1d取样测定。
1.2.8.2微生物指标测定
参照GB4789.2-2022《食品安全国家标准食品微生物学检验菌落总数测定》,样品每隔1d取样,梯度稀释后进行涂布,于37℃培养48h后计数。
1.2.8.3感官质量评定
感官质量评定遵循GB/T22210-2008《肉与肉制品感官评定规范》。挑选10名受过培训人员组成感官评定小组,分别对感官指标进行综合评定。结果均采用10分法呈现,评价标准见表2。
表 2 冷鲜肉感官评定标准
| 指标 | 10~8分 | 6~8分 | 4~6分 | 2~4分 | 0~2分 |
|---|---|---|---|---|---|
| 色泽 | 鲜亮有光泽 | 较鲜亮有光泽 | 暗红无光泽 | 暗灰无光泽 | 暗褐无光泽 |
| 气味 | 鲜味强无异味 | 鲜味较强无异味 | 鲜味淡略有异味 | 无鲜味儿异味较大 | 无鲜味,重异味且不能接受 |
| 弹性 | 弹性很好,指压后立即恢复 | 弹性较好,指压后可以恢复 | 弹性较差,指压后缓慢恢复 | 弹性基本丧失,指压后不能恢复 | 无弹性,指压后凹陷明显不恢复 |
| 粘度 | 外部微湿不黏手 | 外部湿润不黏手 | 外部干燥微黏手 | 外部干燥较黏手 | 外表有粘液很黏手 |
| 大理石纹理 | 纹理清晰,花纹丰富 | 纹理清晰,花纹丰富 | 纹理不清晰,花纹微丰富 | 纹理模糊,有少量花纹 | 无纹理 |
1.2.8.4理化指标测定
肉色采用色差仪测定L*,a*,b*值,每组测定5个不同点;样品pH使用插入式pH计测量,每组测量三次;挥发性盐基氮(TVB-N)含量的测定参考GB5009.228-2016《食品中挥发性盐基氮的测定》中自动凯氏定氮仪法进行测定;参照GB2707-2016《食品安全国家标准鲜(冻)畜、禽产品》中标准TVB-N值>15mg/100g,即为变质肉。以TVB-N值为15mg/100g和菌落总数为106CFU/g作为判断货架期终点的界限。
硫代巴比妥酸(thiobarbituricacidvalue,TBARS)值:称取10.0g搅碎的猪肉样品,加50mL7.5%三氯乙酸溶液(含0.1%乙二胺四乙酸),1000r/min振荡混匀30min,双层滤纸过滤2次,均弃初滤液。取5mL滤液与5mL0.02%硫代巴比妥酸水溶液混合,90℃水浴40min。冷却至室温后1600r/min离心5min,取8mL上清液与5mL三氯甲烷于试管中混匀,静置分层取上清液。以样品空白调零,测定532nm和600nm处光度值。平行测定3次。TBARS含量以每公斤肉的丙二醛毫克数(MDA)表示,计算公式如下:
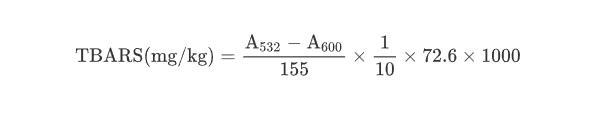
式中:丙二醛与硫代巴比妥酸反应物的消光系数155(mmol·L-1)−1·cm−1。
1.3数据处理
每组实验重复测定3次,结果用平均值±标准差表示;试验数据采用GraphpadPrism9软件作图,以SPSS24软件采用双尾t检验对数据进行显著性差异分析(P<0.05)。
2.结果与分析
2.1不同乳酸菌菌液与其热灭活菌液的抗菌活性
牛津杯法检测到各乳酸菌菌株发酵菌液对指示菌均有一定抑制生长的作用,抑杀单增李斯特菌比大肠杆菌效果好。如图1显示,Lab5菌株对单增李斯特菌抑菌效果最好,抑菌圈为38.28±1.97mm。研究经热灭活处理的乳酸菌液对指示菌抑菌效果发现,经121℃下25min热灭活处理后的菌液仍有较高的抑菌活性。Lab5热灭活与未做处理的菌液相比,抑菌圈直径为36.43±2.06mm。副干酪乳杆菌Lab5菌液与其热灭活菌液对单增李斯特菌的抑菌活性无显著差异(P>0.05),说明热灭活处理不影响其对单增李斯特菌的抑菌能力。副干酪乳杆菌Lab5菌液抑菌圈直径极显著大于热灭活菌液抑菌圈直径(P<0.001),这一差异可能源于活菌不仅代谢产生有机酸和细菌素等多种抗菌物质,还可以通过菌体的生长繁殖和竞争排斥等作用来促进抑菌效果的产生,且后生元与活菌相比,无需冷藏,容易储存且保质期长、携带方便。
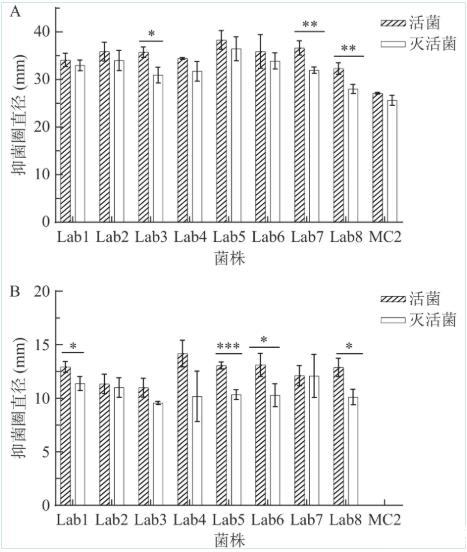
图 1 热灭活与非灭活乳酸菌液对指示菌生长影响
注:A图:指示菌ListeriamonocytogenesATCC19115,B图:指示菌EscherichiacoliATCC25922;图中“*”、“**”、“***”分别代表同一菌株活菌与热灭活菌对指示菌(ListeriamonocytogenesATCC19115或EscherichiacoliATCC25922)抑菌圈直径差异的不同显著性,即P<0.05,P<0.01和P<0.001。
相关新闻推荐
1、在线监测散射光与荧光的微滴度板高通量发酵系统:BioLector的方法验证与应用(五)
