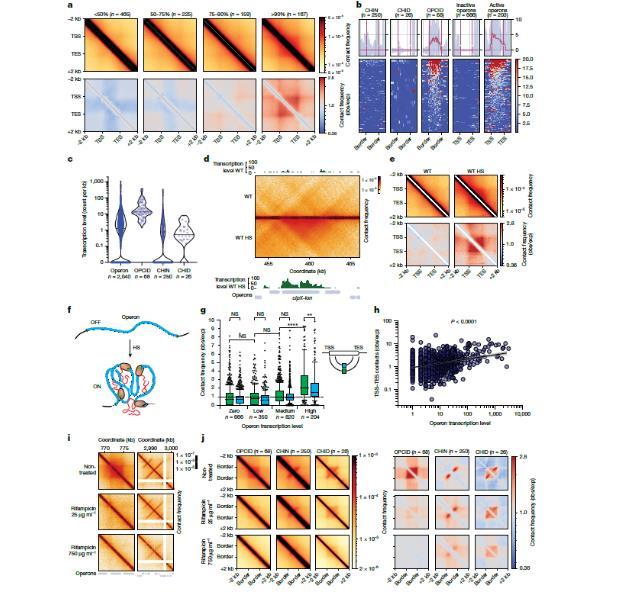
图2、活性纵子上的转录驱动OPCIDs以及抑制基因组区域中转录非依赖性CHIN和CHID。a)基于Red-C信号的按转录活性分组的纵子的平均接触图。b)CHIN、CHID、OPCID、非活性纵子(Red-C信号为零)和活性纵子(Red-C信号排名前10%)周围的转录水平。c)指定基因组特征内的转录水平,按特征长度归一化。d)在正常和HS条件下存在热休克(HS)纵子clpX-lon的区域的接触图。e)正常和HS条件下σ32个纵子的平均接触图。f)示意图说明了在HS条件下转录激活时纵子组装到OPCID中的过程。g)按Red-C信号分为非转录(零Red-C信号)、低转录(底部50%不包括零)、中度转录(50-90%)和高度转录(前10%)的纵子的启动子-终止子接触频率。h)纵子转录水平与启动子-终止子接触频率之间的相关性。黑线表示线性回归,阴影区域表示95%CI。i)含有OPCID和CHIN的两个代表性区域的接触图,显示了用25μg ml-1或750μg ml-1 Rif处理前后的接触图。j)暴露于低浓度(25μg ml−1)或高浓度(750μg ml−1)的Rif前后OPCID、CHIN和CHID的平均接触图,说明了转录抑制对这些基因组结构的影响。
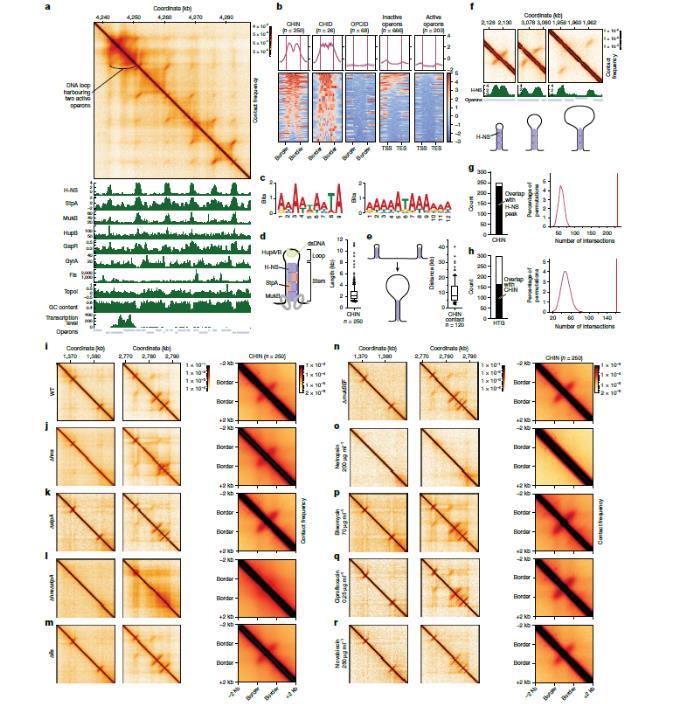
图3、由H-NS和其他国家行动方案指导的CHIN和CHID的组织情况。a)带有NAP分布、GC含量、转录信号和纵子轨迹剖面图示例。b)H-NS在CHIN、CHID、OPCID、非活性纵子和活性纵子周围的分布。c)来自PRODORIC数据库的H-NS基序(左)以及由HOMER鉴定的CHIN基序(右)。d)描述单个CHIN组织的模型,显示了CHIN长度分布。e)一个模型,说明两个CHIN之间的相互作用,它们展开并融合形成一个大环的茎。f)H-NS在CHIN茎区域的定位,在CHIN茎处显示峰值。g)与H-NS峰重叠的CHIN数量。h)与CHIN重叠的HTG数量。i–r,WT E中两个具有代表性的CHIN藏匿区域的接触图。大肠杆菌细胞(i)和指定基因缺失的菌株(j-n)或用抗生素处理的WT细胞(o-r)中的相同区域,说明了Δhns细胞中的CHIN重组和ΔhnsΔstpA和netropsin处理的细胞中的CHIN完全分解。
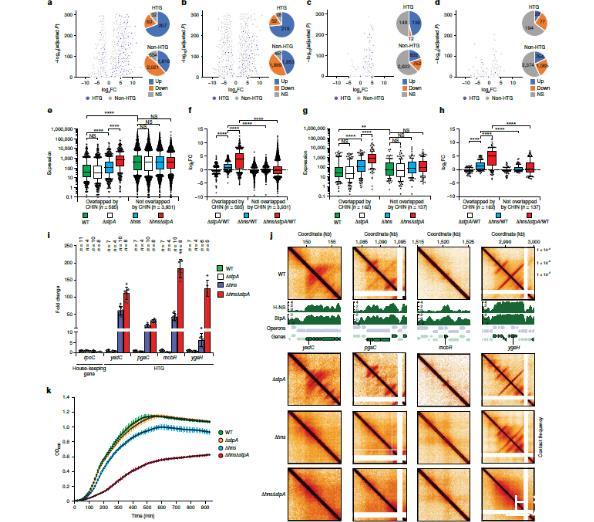
图4,HTG在H-NS和双hns stpA敲除上的激活。a-d)通过RNA测序确定的hns和stpA缺失(a),暴露于200μg ml−1 netropsin(b),hns缺失(c)和stpA缺失(d)后的基因表达变化。e)WT大肠杆菌细胞中与CHINs重叠的基因和与CHINs不重叠的基因的表达水平(绿色)与Δhns(蓝色)、ΔstpA(白色)和ΔhnsΔstpA(红色)中相同基因组的表达水平的比较。f)CHIN相关基因和CHIN非相关基因响应Δhns、ΔstpA和ΔhnsΔstpA的表达变化。g,h)与面板e和f类似,但特别关注HTG。指示基因数(n)。j)Micro-C接触图表示,这些区域含有HTG的区域,在WT、ΔstpA、Δhns和ΔhnsΔstpA细胞中选择用于RT-qPCR分析。k)使用Bioscreen测量的WT、ΔstpA、Δhns和ΔhnsΔstpA大肠杆菌细胞的生长速率。
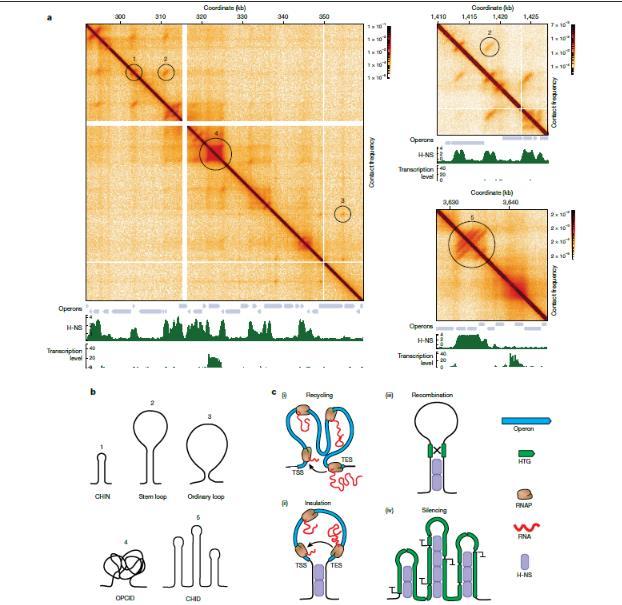
图5,Micro-C在大肠杆菌基因组中捕获的基本和高阶结构。a)来自WT大肠杆菌细胞的接触图示例,显示各种接触模式。b)不同接触模式的解释。c)OPCID和CHIN网络,0可以通过使启动子(TSS)和终止子(TES)靠近(i和ii)来促进RNAP回收。它们还可以建立活性纵子的空间绝缘(ii),实现远处HTG之间的重组(iii)并促进HTG沉默(iv)。
总结
本研究通过开发超高分辨率(10 bp)的Micro-C染色体构象捕获技术,首次揭示了大肠杆菌(E.coli)基因组的三维(3D)精细结构,包括染色体发夹(CHINs)和染色体发夹域(CHIDs)等基本空间单元。这些结构由组蛋白样蛋白H-NS和StpA组织,在抑制水平转移基因(HTGs)中发挥关键作用。研究发现,H-NS缺失会导致3D基因组重组并减弱CHINs/CHIDs,而H-NS/StpA双敲除则完全破坏这些结构,伴随HTGs的转录激活和生长延迟。此外,转录活跃的基因形成操作子大小的染色体互作域(OPCIDs),其结构与转录活性直接相关,表现为Micro-C图谱中的方形接触模式。研究揭示了大肠杆菌核样体的基本结构元素,强调了它们与核样体相关蛋白和转录机制的联系。这些发现不仅增进了对细菌基因组三维组织的理解,还为研究基因表达和基因组稳定性提供了新的视角。通过揭示CHINs和CHIDs在基因沉默中的作用,以及OPCIDs在转录中的作用。
Bioscreen C全自动微生物生长曲线分析仪在本研究中作为表型监测核心工具,通过标准化、自动化培养监测,为3D基因组结构的生物学功能(如H-NS介导的转录调控)提供了关键生长表型数据。其应用贯穿突变体验证、药物处理及环境应激实验,是连接分子机制与宏观表型的重要技术环节。本研究为未来的研究提供了新的方向,特别是在探索细菌如何通过三维基因组结构来调控基因表达和进化方面。提出细菌基因组3D组织的“二元模型”——活跃(OPCIDs)与沉默(CHINs/CHIDs)结构并存,为理解抗生素(如netropsin)靶向NAPs的机制提供新视角。
相关新闻推荐
2、基于β-半乳糖苷酶Lac Z的UPR响应指示菌株的构建及生长曲线测定——材料与方法
